2. Путем решения системы (64) — (71)
определяется выход
ная концентрация метанола t/n+i.
3. Проверяется условие (81). Если оно выполняется, решение на этом заканчивают и значения V\l) и Vi ) считают окончательными.
4. Если заданная точность вычислений не достигнута, пере
ходят к следующему циклу итераций.
Для этого предыдущие значения V\ и V2 увеличивают (при t/n+i < У0) или уменьшают (при у^ >у°) на б и повторяют порядок
расчета, описанный на первой итерации, и т. д. Причем, как только направление изменения V\ и V2
сменится на
противоположное, шаг на этой итерации выбирают вдвое меньше (6(S)='6(S~1V2).
5. На каждой последующей итерации шаг уменьшают вдвое
по сравнению с предыдущим, а направление изменения V\ и V2
определяется
аналогично п. 4.
Последующий этап решения задачи — определение количества греющего пара, необходимого для обеспечения заданной выходной концентрации метанола.
В процессе регенерации пар расходуется на подогрев начальной смеси до ее температуры кипения и на кипячение смеси в кубе колонны:
N = NH + NK, (82)
где NH — расход греющего пара на нагрев начальной смеси, кг/ч; NK — расход греющего пара на кипячение жидкости, кг/ч; N — общий расход греющего пара, кг/ч.
На нагрев жидкости в кубе расходуется теплоты:
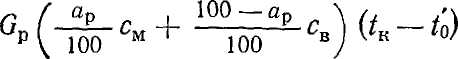
Откуда
— ар
![]() Na =------ ^------------ ^---------- L----------- .------------ .(83)
Na =------ ^------------ ^---------- L----------- .------------ .(83)
Здесь Я — теплосодержание греющего пара, ккал/(кг-°С); 9 — температура конденсата, °С; см, св — теплоемкость соответственно метанола и воды, ккал/(кг-°С); /к — температура кипения смеси в кубе, °С; to — температура поступающей в куб смеси, °С.
Расход теплоты на кипячение смеси в кубе колонны:
Откуда получим
ЛГ„=-&±&±ЙС&_, (84)
где Qo — теплосодержание остатка в кубе, ккал;
157
|
|
«.-О.
t0 — температура кубового остатка, °С; QH — теплота, отдаваемая флегмой хладоносителю в дефлегматоре, ккал;
100-qn+1 ^ . + в 100 ) '
тм, тв — скрытая теплота парообразования соответственно метанола и воды, ккал/кг; Qn — теплота, уносимая парами дистиллята, ккал:
|
100 |
П —П Гт an+i , _. ЮР —an+i I
100
|
|
100 ) cpJ'
^ср — средняя температура паров, поднимающихся с верхней тарелки колонны, °С.
Значение ап+\ получают перерасчетом молярной концентрации xn+i по формуле
А/1
- 100.
Таким образом, математическая модель процесса регенерации метанола представляет собой систему уравнений (64) — (71)
и (80) —(84).
|
Дефлегматор |
|
Тар ел на п |
При решении уравнений модели определяем неизвестные величины Fn+l,
Л-п+Ь ■» о» -^о» ■*») *оБлок-схема модели приведена на рис. 39.
|
Таремна 1 |
|
Уо |
|
Кубколонны |
|
Нагрев и кипячение жидкости в кубе |
|
Хр |
|
Рис. 39. Блок-схема математической модели процесса регенерации метанола |
|
ных переменных Fp, x |
|
p, xp, |
Задача регулирования процесса регенерации метанола рассматривается в соответствии со схемой управления процессом (см. рис. 9) для двух управляющих переменных: расхода флегмы на орошение FN и расхода греющего пара N. Задача регулирования процесса заключается в определении оптимального значения F*N Для каждого набора ВХОД-
|
при котором функционал |
t
158
J=Fn+JFp, определяющий относительную производительность установки по регенерированному метанолу, принимает максимальное значение при выполнении технологических ограничений и требований к качеству продукции.
Математически постановка задачи регулирования записывается следующим образом:
J = Fn+1/Fp -> max, где {Si} — множество допустимых значений, определяемое ограничениями на качество продукции:
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.