7.8. Зарождение и рост новой фазы
7.8.1. Движущая сила при переходе системы в состояние равновесия
Пусть
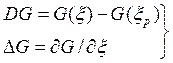 -
обозначения. (7.20)
-
обозначения. (7.20)
Величина ¶G/¶x называется движущей силой процесса установления равновесия (G – энергия Гиббса, x - параметр возмущения термодинамической системы, ξр – значение параметра в равновесном состоянии системы).
Если отклонение
от равновесия невелико, то G(x) можно разложить в
ряд Тейлора в окрестности точки xр
с учётом, что в точке равновесия ![]() :
:
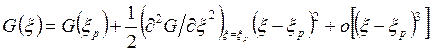 . (7.21)
. (7.21)
Отсюда (учтём,
что G(xр) = const,
![]() )
)
![]() . (7.22)
. (7.22)
Выражая из (7.21) DG = G(x) – G(xр),можно получить
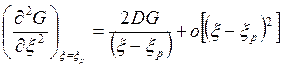 . (7.23)
. (7.23)
Подставляя (7.23) в (7.22), получаем
![]() . (7.24)
. (7.24)
Это общее соотношение для движущей силы процесса установления равновесия.
7.8.2. Минимальный размер зародыша новой фазы
Чтобы при заданной движущей силе процесс образования новой фазы имел место, необходим определённый размер зародыша.
В отсутствии новой фазы зародыши этой фазы образуются за счёт атомных (молекулярных) флуктуаций в виде включений очень малых размеров.
Существует некий критический размер зародыша, ниже которого новая фаза при заданной движущей силе не образуется, а выше - образуется.
При образовании новой фазы затрачивается работа на создание новой поверхности
![]() , (7.25)
, (7.25)
где s - поверхностное натяжение между фазами зародыша β и матрицы a, dА – приращение поверхности.
Можно установить, что при образовании зародыша
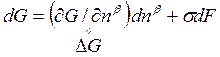 . (7.26)
. (7.26)
Если зародыш – сфера радиусом r, то
![]() , (7.27)
, (7.27)
![]() , (7.28)
, (7.28)
где nβ – число молей вещества в фазе β,
![]() - молярный объем вещества в фазе β
- молярный объем вещества в фазе β
Следовательно,
![]() , (7.29)
, (7.29)
DG = ¶G/¶nb -химическая движущая сила, определяемая соотношением (7.24).
Если ![]() , то
, то ![]() , так
как
, так
как ![]() .
.
Величина DG < 0, а s > 0, поэтому функция (7.29) имеет максимум Gmax(r) = G(rc) (см. рис. 7.9.)
При r < rc – зародыши нестабильны (G - увеличивается с увеличением r).
При r > rc – зародыши стабильны и растут. rc находится из (7.29) на основании условия
![]() , (7.30)
, (7.30)
![]() . (7.31)
. (7.31)
Необходимая энергия для достижения rc (энергия активации) определяется путём подстановки (7.31) в (7.29) ®
![]() . (7.32)
. (7.32)

Таким образом, чем выше s, тем больше rc[см. (7.31)]; чем выше (¶G/¶x), тем меньше rc.
8. Равновесия фаз в многокомпонентных системах
8.1. Общий метод анализа равновесия фаз
1. Производится уточнение, по каким компонентам и фазам систему можно считать не взаимодействующей (скорость изменения этих компонентов очень мала или равна нулю по сравнению со скоростью изменения остальных).
2. Принимается минимальный размер системы, в рамках которой происходит интересуемый процесс и которую можно считать закрытой гетерогенной системой.
3. В рамках закрытой многокомпонентной гетерогенной системы, состоящей из α, β, … θ фаз, выделяются открытые многокомпонентные системы (которые могут быть гетерогенными), взаимодействующие между собой в рамках общей закрытой системы.
4. Далее используются общие критерии равновесия для закрытой системы и частные условия для каждой из однокомпонентных открытых систем.
8.2. Условия равновесия закрытой многофазной системы
Пусть имеем закрытую гетерогенную систему, состоящую из гомогенных открытых систем (фаз). α, β, … θ - фазы гетерогенной системы, n1n, n2n, … nmn - содержание компонентов 1 ... m в фазе n.
Критерий равновесия для этой закрытой системы в соответствии с (3.16):
![]() .
.
Пусть объём и энтропия всей системы неизменны (S, V = const), тогда условие равновесия можно записать в виде
![]() . (8.1)
. (8.1)
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.