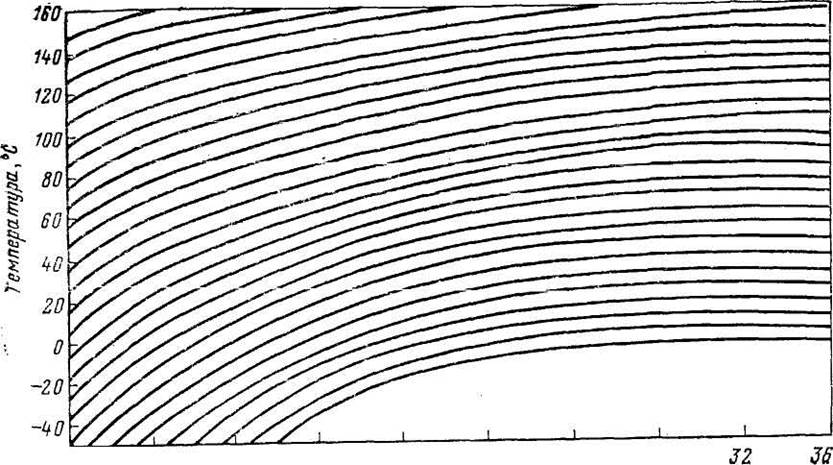
На рис. 35 приведена номограмма, построенная Э. Будагяном на основании энтальпийной диаграммы для метана. Ею можно пользоваться для определения интегрального дроссель-эффекта для природных газов, содержащих метана не менее 90%. Для иллюстрации использования номограммой приведен пример расчета.
Пример V.I. Вычислить дроссель-эффект для природного газа. Начальное давление газа pi=16 МПа, начальная температура 39 °С. Газ подвергается расширению до давления р2=8 МПа.
Решение. В номограмме находят точку с координатами, соответствующими начальным давлению и температуре. Затем эта точка перемещается параллельно ближайшей кривой изоэнтальпии до значения конечного давления. По ординате этой точки находят температуру. Она равна 10°С. Зная значения ри р2, Тх и Т2, по уравнению (V.2) определяют дроссель-эффект (коэффициент Джоуля—Томсона)
136
|
Z8 |
|
■I"? |
 16- 20
16- 20
Давление, МПа
гч
Рис. 35. Диаграмма для расчета процесса дросселирования газа
В работе [27] для расчета коэффициента Джоуля—Томсона для природных газов обосновано использование уравнения
4,19
кр
![]() Ркр
Ркр
Ркр
![]() KD
KD
![]() -рем
-рем
рем!
(V.3)
где
Ркр
pсм — обобщенная функция, в зависимости от приведенных пара-
|
|
метров газа определяемая по рис. 36; Срсм —молярная теплоемкость смеси, кДж/(кмоль-°С)
|
(V.4) |
v-> псм----- '
где СРо — молярная теплоемкость газа при атмосферном давлении, кДж/(кмоль-°С); Ср — изометрическая поправка теплоемкости на давление, кДж/(кмоль-°С), определяемая по графикам (см. рис. 7).
![]() Рис. 36. Зависимость обобщенной функции
Джоуля—Томсона от приведенных дяиления (рПр)
и температуры (Тпр)
Рис. 36. Зависимость обобщенной функции
Джоуля—Томсона от приведенных дяиления (рПр)
и температуры (Тпр)
Пример V.2. Вычислить коэффициент Джоуля Томсоиа для природного газа следующего молярного состава, %:
|
сн4 92,5 |
С3Н8 /-C4H10 /2-C4H10 C5H12
CO2 Nj»
1,5 40 0,4 0,3
1,6 0,25
Параметры газа: р=1б МПа; Г=39°С.
Решение. 1. Определяют псевдокритические параметры смеси. Результаты расчета даны в табл. 58.
Таблица 58
Исходные данные для расчета дроссель-эффекта
|
Компоненты |
Молярные доли |
Гкр. К |
Ркр, МПа |
Т У ■ кр i |
РкрГ1 |
Ср о < кДж/кмоль |
Yfpo |
|
сн4 |
0,9250 |
190,5 |
4,67 |
176,2 |
4,3197 |
35,6 |
32,94 |
|
СгНв |
0,0300 |
306 |
4,94 |
9,2 |
0,1482 |
52,0 |
1,56 |
|
СзНв |
0,0150 |
369,6 |
4,42 |
5,5 |
0,0663 |
69,6 |
1,04 |
|
/-С4Н10 |
0,0040 |
407 |
3,89 |
1,6 |
0,0156 |
87,2 |
0,35 |
|
л-С4Н]0 |
0,0045 |
425 |
3,64 |
1,9 |
0,0164 |
87,2 |
0,39 |
|
л-С5Н12 |
0,0030 |
460,7 |
3,35 |
1,4 |
0,0101 |
104,8 |
0,31 |
|
СО2 |
0,0160 |
304,1 |
7,43 |
4,9 |
0,1189 |
37,3 |
0,60 |
|
N2 |
0,0025 |
126 |
3,41 |
0,3 |
0,0085 |
29,3 |
0,07 |
|
Итого |
1,0000 |
201,0 |
4,7037 |
37,26 |
Согласно данным табл. 58, ркр = 4,70 МПа; Гкр = 201 К-
2. Определяют удельную
молярную теплоемкость газа. Результаты рас
чета также сведены в табл.
58, СРо=37,26 кДж/кмоль.
3. Рассчитывают приведенные параметры газа:
Т -Л1-1 55 1пр — 9П] — ' »
|
|
|
рпр л -г о,4. |
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.