Энтропию по методу РКБ определяют по уравнению
|
Rr In (l + -j-) + R In |
z — т R
(1.22)
где SCM — энтропия реальной смеси; SCu о— энтропия идеальной смеси; т — коэффициент, определяемый по уравнению (1.19); г — коэффициент, определяемый по формуле
;. U934 — Dt + Ct
(1.23)
Т а б лица 10
Значения коэффициентов Бг и Сг для уравнения (1.18)
|
Коэффициенты |
Коэффициенты |
||||
|
Компоненты |
Компоненты |
||||
|
Bi |
ci |
||||
|
Л.чот |
7,66 |
1 0,30 |
Гексаи |
10,0 |
1,4 |
|
Метан |
7,50 |
0,35 |
Гептан |
10,5 |
1,3 |
|
Этан |
8,20 |
0,70 |
Октан |
11,0 |
1,4 |
|
Пропан |
8,82 |
0,50 |
Нонан |
11,2 |
1,4 |
|
f-Бутан |
8,80 |
1,0 |
Декан |
11,6 |
1,4 |
|
п-Бутан |
8,90 |
1,0 |
Углекислый газ |
9,8 |
0,3 |
|
г-Пентан |
9,4 |
1,25 |
Сероводород |
8,3 |
0,8 |
|
я-Пентан |
9,5 |
1,25 |
|||
:28
Значения коэффициентов В{ и С*, входящих в уравнение (1.18), даны в тябл. ш,
Энтропия i-ro компонента в идеальном состоянии определяется по уравнению
![]() 10*
10*
"ГзЛ|Ю6 ~ 4
Г4— 1
![]() 108
108
_6_
5
до10
Н-
(1.24)
Вязкость. Вязкость характеризует свойства частиц, жидкостей или газов сопротивляться взаимному перемещению.
Физические причины вязкости заключаются в молекулярных силах, действующих как сила сцепления между частицами тел, которая проявляется при наличии относительного перемещения соседних слоев жидкости или газа.
Абсолютную вязкость отдельных газов при атмосферном давлении в зависимости от температуры можно определять по рис. 8.
Ппи определении вязкости газовых смесей fiCM руководствуются правилом аддитивности
где Yi — молярная концентрация i-ro компонента в смеси; \ц — вязкость того же компонента.
Вязкость отдельных газов при атмосферном давлении может определяться по формуле
![]() = 0,002669
= 0,002669
(1.26)
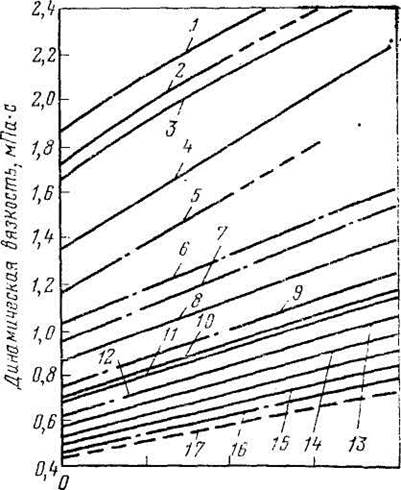 Рис. 8. Зависимость динамической вязкости
газов при атмосферном давлении от
температуры:
Рис. 8. Зависимость динамической вязкости
газов при атмосферном давлении от
температуры:
/ гелии; 2 — воздух; 3 — азот; 4 — углекислый газ; 5 — сероводород; 6 — метан; 7 — этилен; 8 — этан: 9 — пропан: 10 — н-бутан; //— и-бутан; 12 — н-пентан; 13 — н-гексан; 14 — н-гептан; 15 — н-октан; 16 — н-нонан; 17 — н декан
50 100 150
Температура, "С
ZOO
29
где а — параметр межмолекулярного взаимодействия, значения для компонентов даны в табл. 3; Q — интеграл столкновений.
Для неполярных веществ, к которым относятся углеводороды^ азот и двуокись углерода, значения Q в зависимости от Т* даны в табл. I i, где
T* = T/{bIK)i. (I.27)
Таблица 11
Значения интеграла столкновений Q при различных Т* для неполярных компонентов [22]
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.