![]() — скорость стадии -той реакции.
— скорость стадии -той реакции.
По закону действующих масс:
![]()
где
![]() — константа скорости -той реакции;
— константа скорости -той реакции;
![]() — концентрации.
— концентрации.
Общий порядок реакции равен;
![]()
где ![]() зависит от температуры:
зависит от температуры:
![]()
где ![]() — предэкспоненциальный множитель, зависящий от
свойств компонентов;
— предэкспоненциальный множитель, зависящий от
свойств компонентов;
![]() — энергия активации -той реакции;
— энергия активации -той реакции;
Химические реакции по количеству стехиометрических уравнений описывающих их протекание подразделяются на простые и сложные.
Пример простых:
1)
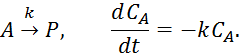
2)
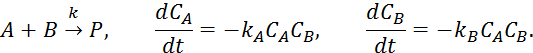
3)
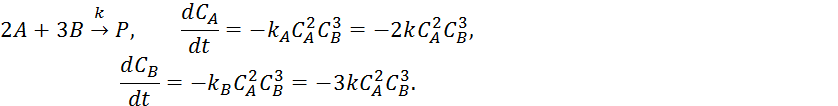
Константы
скорости реакции по соответствующему компоненту равна константе стадии реакции ![]() на
соответствующий стехиометрический коэффициент.
на
соответствующий стехиометрический коэффициент.
Сложные реакции делятся на параллельные, последовательные и смешанные и обратимые. Изменение концентрации -того вещества в сложной реакции равна скорости его образования (расходования) на всех стадиях в которых данное вещество участвует, то есть сложная реакция разделяется на отдельные стадии.
Пример:
1) Параллельная реакция:
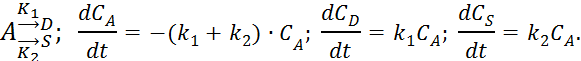
2) Последовательная реакция:
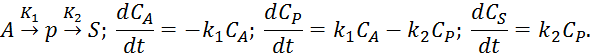
3) Обратимая реакция:
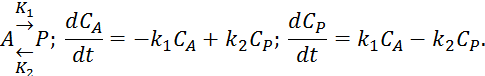
4) Смешанная:
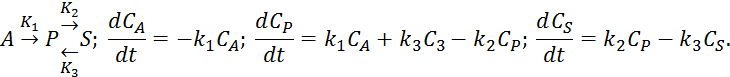
6.2. Математическая модель химического реактора идеального перемешивания
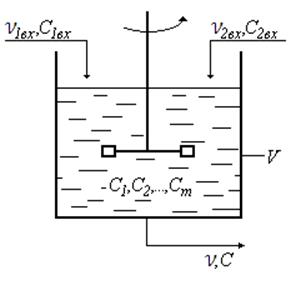
Рис. 36
Вследствие идеального перемешивания концентрация всех компонентов на входе из реактора постоянна.
![]() — плотность всех компонентов поступающих в реактор;
— плотность всех компонентов поступающих в реактор;
![]() — плотность в реакторе;
— плотность в реакторе;
![]() — объем зоны идеального перемешивания.
— объем зоны идеального перемешивания.
Математическая модель включает уравнение материального баланса по жидкой фазе и по концентрациям каждого -ого компонента.
Материальный баланс по жидкой фазе:

Уравнение материального баланса по изменению -ого компонента:
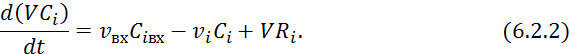
где
![]() — скорость реакции по -ому компоненту;
— скорость реакции по -ому компоненту;
![]() равно сумме скоростей образования и расходования
-ого компонента.
равно сумме скоростей образования и расходования
-ого компонента.
Пусть
в реакторе протекает ![]() реакций:
реакций: ![]()

![]()
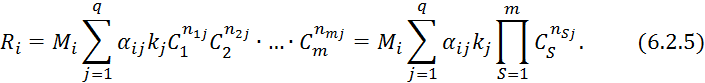
Подставляем 6.2.2 в 6.2.5:
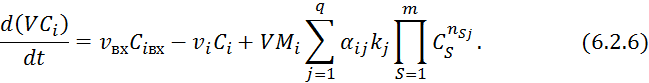
Пример:
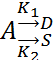
Принимаем, что ![]()
![]()
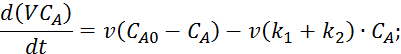
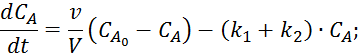
![]()
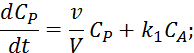
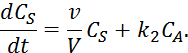
6.3. Математическая модель реактора идеального вытеснения
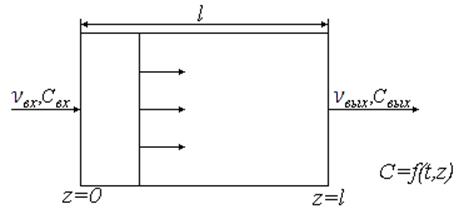
Рис. 37
Математическая модель включает уравнение по потокам и по концентрациям компонентов веществ участвующих реакциях.
Уравнение материального баланса по потокам вещества согласно разделу 3.4 имеет вид:

Изменение концентрации -того вещества определяется двумя факторами:
1) Гидродинамикой процесса;
2) Скоростью химического превращения.
Уравнение материального баланса по измерению концентрации -того вещества имеет следующий вид:

Вместо
![]() подставляем 6.2.5:
подставляем 6.2.5:
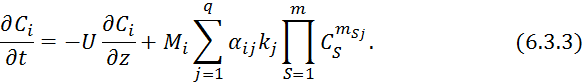
Пример:
![]()
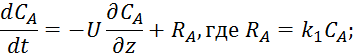
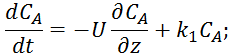
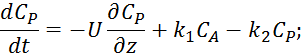
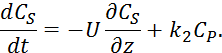
6.4. Передаточные функции химических реакторов
6.4.1. Передаточная функция реактора идеального перемешивания простого типа
![]()
![]()
где
![]() — концентрация исходного вещества.
— концентрация исходного вещества.
Уравнение
материального баланса по компоненте ![]() :
:
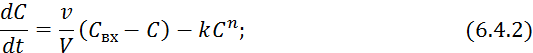
![]()
Принимаем ![]() :
:

![]()
где
![]() — концентрация в любой точке;
— концентрация в любой точке;
![]() — оператор.
— оператор.
Так как
начальные условия не нулевые то оператор ![]() является нелинейным.
является нелинейным.
Для решения
6.4.4 оператор ![]() необходимо привести к линейной форме:
необходимо привести к линейной форме:
![]()
где
![]() — линейный оператор;
— линейный оператор;
![]()
Преобразуем 6.4.4:

Рассмотрим
6.4.7 при ![]() :
:
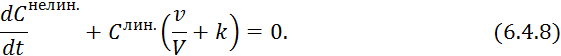
где ![]() — результат действия нелинейного оператора
— результат действия нелинейного оператора ![]() при
при ![]() .
.
![]()
Решение уравнения 6.4.8 при 6.4.9 будет иметь следующий вид:
![]()
Вычитаем из уравнения 6.4.7 уравнение 6.4.8:
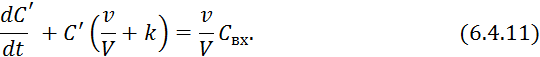
где ![]()
![]()
Преобразуем по Лапласу по времени при начальных условиях 6.4.12 уравнение 6.4.11:
![]()
![]()
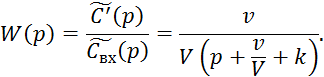
6.4.2. Реактор идеального вытеснения
![]()
![]()
где
![]() — концентрация вещества
— концентрация вещества ![]() .
.
Уравнение модели реактора будет иметь следующий вид:


![]()
![]()
![]()
![]()
![]()
Перепишем 6.4.16 с условием 6.4.20:

![]()
![]()
Преобразуем по Лапласу по времени 6.4.21 при нулевых начальных условиях:
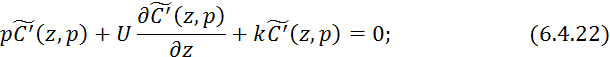
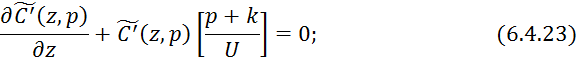
![]()
Решение уравнения 6.4.23 с граничными условиями 6.4.24:
![]() )
)
![]()
Уравнение 6.4.25 при ![]() примет вид:
примет вид:
![]()
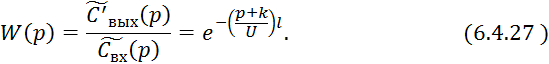
7. Математическое моделирование динамики типовых контуров регулирования технологических параметров объекта
7.1. Свойства, характеристики и классификация объектов регулирования
Свойства объекта регулирования определяют выбор типа регулятора для контура объекта, расчет настроек регулятора, а также является основой синтеза автоматической системы регулирования (АСР).
Основными свойствами являются:
1) самовыравнивание;
2) емкость;
3) запаздывание.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.