Таблица 5.8.
Влияние добавок Э4+(Si, Zr, Ti) на концентрацию электронодонорных и электроноакцепторных центров.
|
образец |
% Э(IV)/Al, по молям |
% ЭO2(IV), по массе |
Nдон.*г-1, 1018 |
Nак.*г-1, 1016 (сильн. центры) |
|
|
γ-Al2О3 |
0 |
0 |
6.60 |
2.61 |
|
|
γ-Al2О3 с Si |
I |
1.6 |
1.8 |
6.47 |
4.60 |
|
γ-Al2О3 с Zr |
1.6 |
3.0 |
3.43 |
4.97 |
|
|
γ-Al2О3 с Ti |
1.6 |
2.4 |
4.30 |
4.71 |
|
|
γ-Al2О3 с Si |
II |
2.4 |
2.8 |
1.80 |
4.36 |
|
γ-Al2О3 с Zr |
2.4 |
5.5 |
0.95 |
3.81 |
|
|
γ-Al2О3 с Ti |
2.4 |
3.6 |
1.49 |
3.40 |
|
5.2.2 Изучение добавок хлорид и сульфат ионов на концентрацию электронодонорных и сильных электроноакцепторных центров для промышленных оксидов алюминия.
Изучение влияния хлорид и сульфат ионов на концентрацию сильных электроноакцепторных и электронодонорных центров проводилось на примере оксида алюминия марки AOK-63-22 (Табл. 5.9).
Таблица 5.9.
Влияние добавок Сl- и SO42- на концентрацию электронодонорных и электроноакцепторных центров.
|
образец |
Nдон.*г-1, 1018 |
Nак.*г-1, 1016 (сильн. центры) |
|
Al2O3 (АОК-63-22) |
2,76 |
4,94 |
|
2 масс. SO42-/ Al2O3 |
2,33 |
5,18 |
|
4 масс. SO42-/ Al2O3 |
1,61 |
7,42 |
|
8 масс. SO42-/ Al2O3 |
0,60 |
16,54 |
|
1 масс. Cl-/ Al2O3 |
2,26 |
6,41 |
|
2 масс. Cl-/ Al2O3 |
1,97 |
6,67 |
|
4 масс. Cl-/ Al2O3 |
1,92 |
8,16 |
Было обнаружено (Рис. 5.9), что при введении SO42- от 0 до 2 масс. % концентрация сильных электроноакцепторных центров практически не изменяется. Дальнейшее повышение количества вводимых SO42- от 2 до 4 масс. % приводит к небольшому росту концентрации детектируемых сильных электроноакцепторных центров. При введении же 8 масс. % SO42- ионов количество сильных электроноакцепторных центров увеличивается более чем в 2 раза.
Концентрация электронодонорных центров, плавно, практически линейно уменьшается с увеличением количества вводимых SO42- ионов от 0 до 8 масс. %.
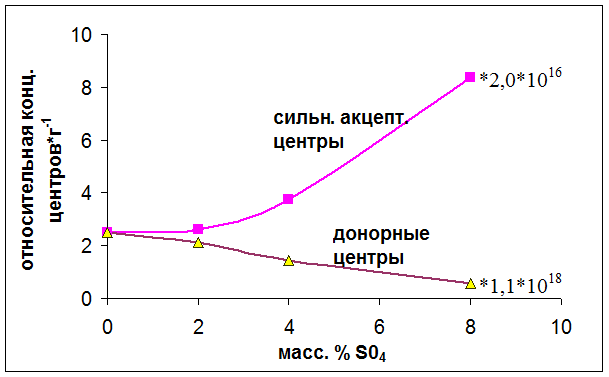
Рис. 5.9. Влияние концентрации SO42- ионов на количество детектируемых сильных электроноакцепторных и электронодонорных центров.
При введении Cl- от 0 до 4 масс. % к оксиду алюминия наблюдалось следующие поведение концентрации электронодонорных и сильных электроноакцепторных центров - Рис. 5.10. Концентрация сильных электроноакцепторных центров практически линейно возрастала с увеличением количества вводимых Cl- от 0 до 4 масс. % Концентрация же электронодонорных центров линейно уменьшалась с увеличением количества вводимых Cl- от 0 до 2 масс. %, после чего 2 – 4 масс. % Cl- практически не изменялась.
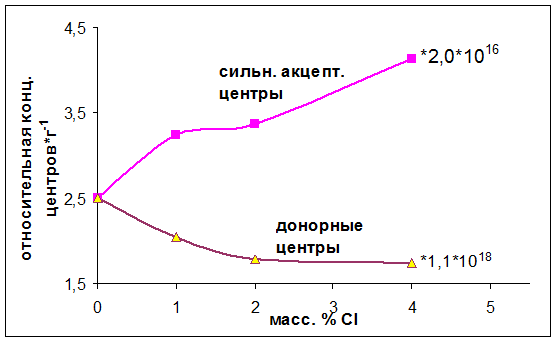
Рис. 5.10. Влияние концентрации Cl- на количество детектируемых сильных электроноакцепторных и электронодонорных центров.
5.3. Корреляционные зависимости между каталитической активностью в реакциях дегидратации спиртов и концентрацией электронодонорных и сильных электроноакцепторных цеторов.
При изучении кислотно-основных и каталитических свойств различных
модифицированных оксидов алюминия, была установлена взаимосвязь между
концентрациями электронодонорных (основных), сильных электроноакцепторных
(кислотных) центров и удельной скоростью образования олефинов (этилена и
бутилена) W[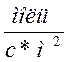 ].
].
Для особо чистых оксидов алюминия, модифицированных оксидами титана, циркония и кремния при изучении процесса дегидратации н-бутанола были получены линейные корреляционные зависимости (Рис. 5.11 – 5.12).
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.