Исследование влияния сульфат ионов на активность оксидов алюминия показало что, введение сульфат ионов в структуру оксида алюминия приводит к резкому увеличению активности в реакции дегидратации. Но время и условия эксперимента были такие, что катализаторы быстро дезактивировались и роста активности практически не наблюдалось (Табл. 5.7). Длительные испытания сульфатировнных оксидов алюминия проводились в более мягких условиях при температуре T=350oC и времени контакта 1 c на примере образца 8 масс. % SO42-/АОК-63-22. На графиках (Рис. 5.8 – 5.9) видно, что активность и селективность сульфатированного образца падает за 6,5 часов почти до уровня индивидуального оксида алюминия, что связано с зауглероживанием катализаторов. Последующая регенерация кислородом и водородом не приводила к восстановлению активности (Рис. 5.8 – 5.9). Следует также отметить, что при изучение процесса зауглероживания катализаторов на основе оксидов алюминия было показано [134], что введение до 2 масс. % SO42- практически не влияет на удельную скорость зауглероживания.
Таблица 5.7.
Влияние добавок сульфат ионов на активность оксидов алюминия в реакции дегидратации этанола
|
Шифр образца |
% масс. SO42- |
T=350оC |
|||
|
Х C2H5OH |
S C2H4 |
S АЦА |
S ДЭЭ |
||
|
АОК-63-22 |
0 |
73,6 |
53,1 |
1.2 |
45,7 |
|
4 |
81,6 |
72,7 |
1,6 |
25,7 |
|
|
8 |
80,4 |
70,0 |
1,1 |
28,9 |
|
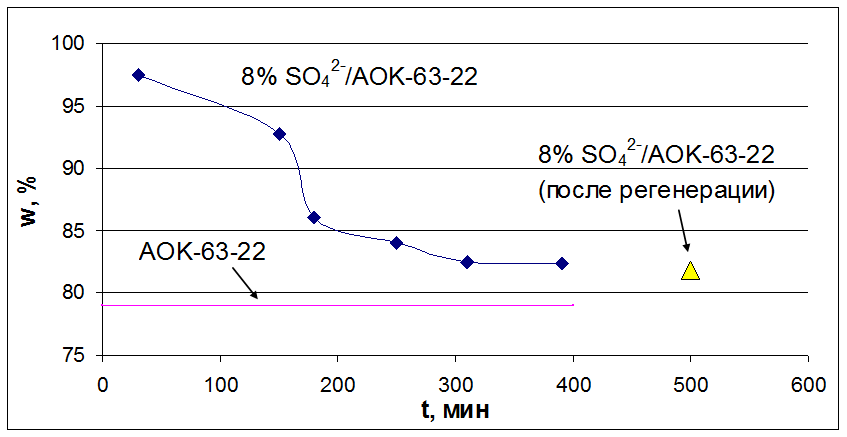
Рис. 5.8. Влияние времени проведения процесса дегидратации на величину конверсии этанола.
Где, w – конверсия этанола; t – время.
Условия испытания: Vкат. =1см3; T=350оC; τ (время контакта) = 1,0 c.
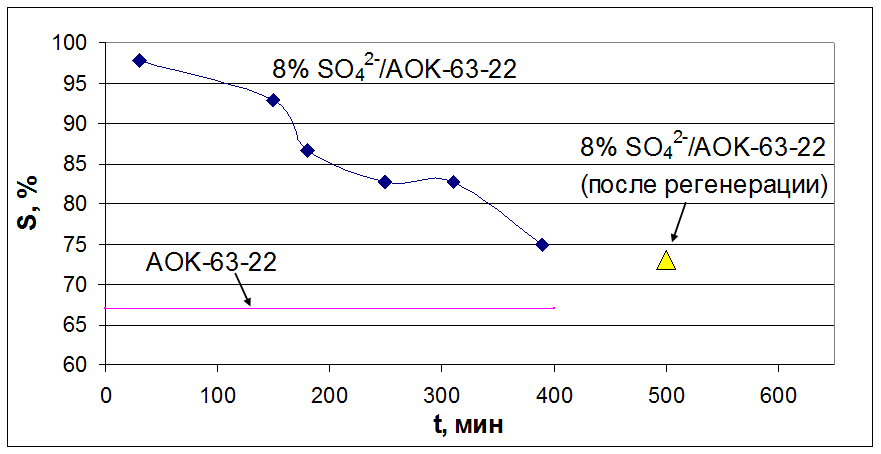
Рис. 5.9. Влияние времени проведения процесса дегидратации на селективность по этилену.
S – селективность по этилену; t – время.
Условия испытания: Vкат =1см3; T=350оC; τ (время контакта) = 1,0 c.
5.2. Изучение влияния добавок модифицирующих элементов на концентрацию электронодонорных и сильных электроноакцепторных центров оксидов алюминия
Определение концентрации электронодонорных (основных) центров проводилось по адсорбции тринитробензола. Концентрация сильных электроноакцепторных (кислотных) центров определялась по адсорбции п-ксилола и толуола. В дальнейшем будут употребляться термины - электронодонорные и электроноакцепторные центры, подразумевая, что они соответственно связаны с поверхностными основными и кислотными свойствами оксидов.
5.2.1. Изучение влияние добавок четырехвалентных элементов на концентрацию электронодонорных и электроноакцепторных центров особо чистых γ-Al2O3.
Было изучено влияния добавок четырехвалентных элементов (Si, Ti, Zr) на концентрацию электронодонорных и сильных электроноакцепторных центров особо чистых оксидах алюминия, приготовленных по алкоголятной технологии .
Еще до снятия спектров ЭПР, по изменению цвета раствора можно было качественно судить об относительной основности и кислотности образцов. Результаты ЭПР подтвердили первоначальные выводы и дали представления о количестве этих центров (Табл. 5.8).
Как мы видим из таблицы 5.8, введение одинакового атомного количества четырехвалентных элементов в кристаллическую структуру оксида алюминия приводит к уменьшению количества электронодонорных центров в следующем порядке Si>Ti>Zr, как в первой серии образцов (I), так и во второй (II), в которой содержание вводимых Э(IV) было увеличено в 1,5 раза. Наибольшая концентрация электроноакцепторных центров в первом случае (I) у образца с добавкой циркония, а во втором (II) у образца с добавкой кремния, что можно объяснить различной удельной поверхностью этих оксидов. Если же полученные данные пересчитать на единицу поверхности наибольшая концентрация электроноакцепторных центров (Nак.*м-2) как в первой, так и во второй серии будет именно у образцов с добавкой циркония. Индивидуальный гамма оксид алюминия, из всех вышеприведенных (Табл. 5.8) содержит наибольшее количество электронодонорных и наименьшее количество сильных электроноакцепторных центров.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.