Для определения объема фракции – величины, необходимой для расчетов, в мерный цилиндр количественно перенести содержимое 10-15 фракций, замерить объем и рассчитать объем одной фракции, Vфр..
Измеряют линейкой величины диаметра колонки и высоты столба геля в колонке, откуда рассчитывают объем Vt.. Измеряют также длину и внутренний диаметр шланга, идущего от колонки к коллектору, и рассчитывают его объем.
Строят профиль элюции, откладывая на оси абсцисс номер фракции, а на оси ординат – оптическую плотность. Определяют по графику номера фракций Nфр., соответствующих максимальному значению оптической плотности для каждого из трех пиков.
В соответствии с рис.5, рассчитывают Ve для каждого вещества как Nфр.·Vфр..
Точное значение Ve получается после вычета поправки 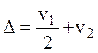 , где v1 – объем нанесенной
пробы; v2 – объем шланга, идущего от колонки к коллектору.
, где v1 – объем нанесенной
пробы; v2 – объем шланга, идущего от колонки к коллектору.
Далее заполняют таблицу:
|
Тип геля |
Сефадекс (или Молселект) |
|
Элюент |
Р-р NaCl 9 г/л |
|
Скорость элюции |
|
|
Время отбора одной фракции |
|
|
Объем одной фракции |
|
|
V0 = Ve декстрана |
|
|
Ve цитохрома |
|
|
Ve хромата |
|
|
Vt – объем геля в колонке |
|
|
Vt –V0 |
По формуле (15) рассчитывают величины Kav для цитохрома С и хромата калия.
Данные свести в таблицу:
Компонент |
Ve, мл |
Ve –V0, мл |
Kav |
|
цитохром С хромат калия |
Оценить ширину пиков w для цитохрома С и хромата калия, как показано на рис.5. Затем по формулам (10) и (11) рассчитать число эффективных теоретических тарелок n и величину ВЭТТ.
Данные свести в таблицу:
|
Компонент |
Ve, мл |
w, мл |
n |
ВЭТТ |
|
цитохром С хромат калия |
5. ЭЛЕКТРОФОРЕЗ
Электрофорез – движение заряженных частиц в растворе под действием электрического поля. При движении заряженной сферической частицы в однородном электрическом поле в отсутствии солей ее электрофоретическая подвижность
U = V/E,
где V – скорость частицы, а Е – напряженность электрического поля.
Электрофоретичеcкая подвижность частицы определяется условием равенства силы, действующей на частицу со стороны поля, и силы трения, обусловленной вязкостью среды:
QE = 6πrηV,
где Q – заряд частицы, r – ее радиус, η – вязкость среды.
Таким образом, для свободного электрофореза непроводящей сферической частицы в диэлектрике
U = V/е = Q/6πrη.
Следовательно, подвижность частицы прямо пропорциональна ее заряду и обратно пропорциональна ее размеру.
В реальных условиях на подвижность заряженной частицы влияют ионная сила раствора (за счет экранировки заряда частицы солями буфера), рН (меняет степень диссоциации, значит и эффективный заряд) и другие факторы.
При электрофорезе в геле подвижность оказывается меньше, чем в случае свободного электрофореза
U/U0 = α,
где Uо – подвижность при свободном электрофорезе, α – коэффициент задержки (α <1).
Коэффициент задержки α является параметром, зависящим от размера пор и природы геля и от размеров и формы разделяемых молекул.
Таким образом, эффект молекулярного сита, лежащий в основе гель-электрофореза, состоит в том, что отдельные молекулы разделяются не только по их общему электрическому заряду, но также и по величине (молекулярный вес) и по форме (пространственная структура).
Э-1. Гель-электрофорез ДНК
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.