5 С2О42- - 2ē → 2СО2
2MnO4- + 5С2О42- + 16Н+ → 2 Mn2+ +10СО2 + 8 H2O
Следовательно, ЭМщ.к. = 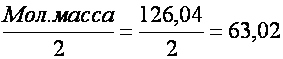
Расчет навески для приготовления первичного стандартного раствора ведут по формуле:
![]() атеор. =
атеор. = ![]() ,
,
где атеор. – навеска, г;
N – нормальность раствора, г-экв/л;
Vк – объем мерной колбы, мл;
ЭМ – грамм-эквивалент.
Для приготовления 250 мл 0,02 н.раствора щавелевой кислоты следует взять навеску:
атеор. = ![]()
Рассчитанное количество щавелевой кислоты взвешивают в бюксе сначала приблизительно на технических весах, а затем точно на аналитических весах.
Щавелевую кислоту через воронку количественно переносят в мерную колбу, растворяют в холодной дистиллированной воде, добавляют воды до метки и тщательно перемешивают. Пустой бюкс взвешивают также на аналитических весах.
Навеска определяется по разности двух взвешиваний (апракт.):
Вес бюкса с навеской - А (г)
Вес пустого бюкса - В (г)
Навеска - апр. (г)
апр. = А – В
Нормальность приготовленного первичного стандартного раствора щавелевой кислоты вычисляют по формуле:
N = ![]() ,
г – экв/л
,
г – экв/л
2. Установление концентрации раствора перманганата калия.
Конценрацию раствора КМnО4 - устанавливают по первичному стандартному 0,02 н.раствору щавелевой кислоты (или оксалата натрия). Раствор КМnО4 наливают в бюретку и устанавливают уровень жидкости на нуле по верхнему мениску (окрашенный раствор). В три конические колбы переносят пипеткой по 10 мл стандартного раствора щавелевой кислоты и добавляют мензуркой по 10 мл 4 н. Н2SО4. Последовательно каждую из колб нагревают до 80-90ºС и раствор медленно при непрерывном помешивании титруют раствором перманганата калия до появления бледно-розового окрашивания.
При титровании идет следующая реакция:
5H2C2O4 + 2KMnO4 + 3H2SO4 → 2MnSO4 + 10CO2 + 8H2O
5C2O42- + 2MnO4- + 16H+ → 2Mn2+ + 10CO2 + 8H2O
Практически эта реакция идет в несколько стадий. Нагревание и повышение концентрации ионов водорода способствует увеличению скорости взаимодействия перманганата с щавелевой кислотой. Ионы марганца (II) оказывает каталитическое действие на реакцию (автокатализ).
Во время титрования раствор перемешивают и каждую следующую каплю добавляют только после исчезновения окраски от предыдущей капли. Титрование проводят не менее 3-х раз до получения сходящихся результатов. Находят среднее значение, по которому рассчитывают точную концентрацию титранта (вторичного стандартного раствора) по формуле:
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.