Известно, что ацетилацетон представляет собой смесь двух изомеров – енольной и кето-формы, которые находятся в равновесии:
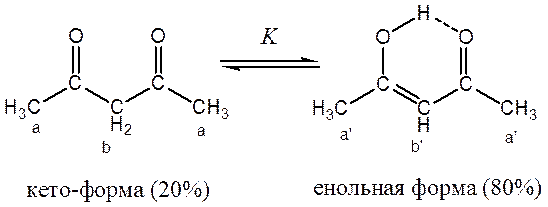
![]()
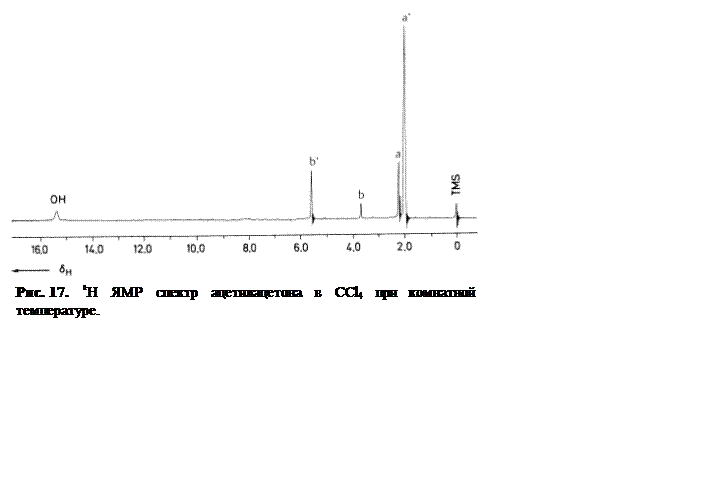
В спектре ЯМР (Рисунок 17) это соответствует двум группам линий, причем кето-форме соответствуют две линии, а енольной форме – три линии. Величина константы равновесия К для процесса кето-енольной таутомерии представляется в виде
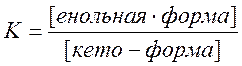 , (9.2)
, (9.2)
Тогда изменение изобарного потенциала для кето-енольной таутомерии можно представить в виде
![]()
или
![]() (9.3)
(9.3)
Выражение (9.3) перепишем следующим образом:
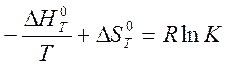
Анализируя
температурную зависимость константы К, можно получить значения ![]() и
и ![]() .
.
Методика проведения эксперимента
1. В 5 мм ампулу ЯМР помещают 0,6 мл ацетилацетона.
2. Записывают протонный спектр ЯМР ацетилацетона при комнатной температуре и производят отнесение линий.
3. Определяют отношение концентраций енольной и кето-форм ацетилацетона при комнатной температуре из отношения интегральных интенсивностей сигналов СH3-групп, иными словами, определяют K по формуле (9.2).
4. Повышают температуру на 5‑8 °С и вновь определяют К.
5. Получают зависимость К = f(Т) в 5‑10 точках до температуры 80 °С.
6. Строят
линейную зависимость RlnK от ![]() по методу наименьших квадратов.
Из отсекаемого отрезка и тангенса угла наклона зависимости RlnK от
по методу наименьших квадратов.
Из отсекаемого отрезка и тангенса угла наклона зависимости RlnK от ![]() получают
получают
![]() и
и ![]() и
определяют величины стандартных отклонений
и
определяют величины стандартных отклонений ![]() и
и ![]() на основании общих выражений, приведённых
ниже.
на основании общих выражений, приведённых
ниже.
![]() (9.4)
(9.4)
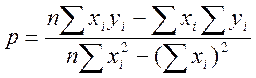 ;
; 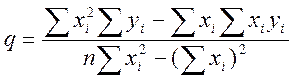 (9.5)
(9.5)
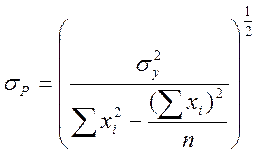 ;
; 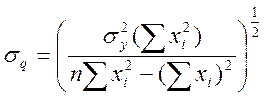 , (9.6)
, (9.6)
где хi и уi – экспериментальные значения х и у; sy определяется уравнением
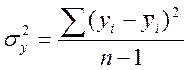
Здесь yi = RlnK, xi = 1/T, p
= −![]() , q =
, q = ![]() , n – число
точек в эксперименте;
, n – число
точек в эксперименте; ![]() – это значения
– это значения ![]() на прямой, определяемой из уравнения
(9.4), с учётом p и q, найденных по МНК и экспериментальных значений xi.
на прямой, определяемой из уравнения
(9.4), с учётом p и q, найденных по МНК и экспериментальных значений xi.
7. Результаты заносят в таблицу
|
Т, К |
К |
|
|
|
|
ЛАБОРАТОРНАЯ РАБОТА Я-2
Измерение константы устойчивости лабильного комплекса хлороформа с трис(ацетилацетонатом) хрома(III) (Сr(асас)3) в четыреххлористом углероде
Установлено, что взаимодействие хлороформа с Сr(асас)3 осуществляется по механизму внешнесферного комплексообразования. Химическая связь в комплексе Сr(асас)3·СНСl3 образуется за счет присоединения CHCl3 к атому кислорода ацетилацетонатного лиганда Сr(асас)3 по типу образования водородных связей
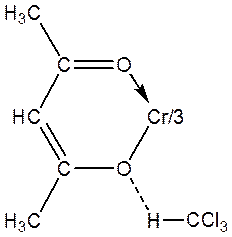 Ширина линии какого-либо ядра в спектре ЯМР определяется
взаимодействием магнитного момента этого ядра с магнитными моментами других
ядер молекулы, а также с магнитными моментами ядер окружающей среды.
Ширина линии какого-либо ядра в спектре ЯМР определяется
взаимодействием магнитного момента этого ядра с магнитными моментами других
ядер молекулы, а также с магнитными моментами ядер окружающей среды.
Комплекс Сr(асас)3 является парамагнитным, т.е. обладает неспаренным электроном. Магнитный момент электрона приблизительно в 1000 раз больше магнитного момента любого ядра, и вследствие этого взаимодействие ядер с неспаренным электроном парамагнитного комплекса металла велико по сравнению с взаимодействиями ядерных магнитных моментов между собой.
Это приводит к уширению сигналов ЯМР ядер, взаимодействующих с парамагнитными металлами. Процесс комплексообразования между СНСl3 и Cr(асас)3 – можно представить в виде одностадийной схемы.
|
![]() ,
,
где М = Сr(acac)3, L = CHCl3, K – константа устойчивости, определяемая как
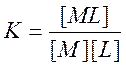 .
.
Комплекс Сr(асас)3·СНСl3 является лабильным. Обмен молекулы СНСl3 между свободным и координированным состоянием осуществляется за времена t » 10−11 с, что соответствует условию быстрого обмена в шкале времени ЯМР. При этом, в спектре ЯМР не наблюдается отдельно линия свободной молекулы СНСl3 и линия молекулы СНСl3 в комплексе Сr(асас)3·СНСl3, а возникает один сигнал, все параметры которого (в том числе и ширина) соответствуют средневзвешенным значениям между параметрами линий свободной и координированной молекулы СНСl3. Для наблюдаемой ширины линии хлороформа (Dn1/2,набл.) в присутствии Сr(асас)3 имеет место следующее выражение по аналогии с выражением (6.3):
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.