|
Давление, кТс/см*1 |
Температура, |
К |
||
|
0 мас.$ CTLOH |
50 мае .5? |
60 тс.% |
70 мае./? |
|
|
127 |
— |
264,5 |
255,5 |
244,0 |
|
120 |
296,3 |
263,2 |
254,0 |
243,0 |
|
100 |
291,3 |
260.6 |
252,3 |
— |
|
40 |
286,3 |
256.1 |
248,7 |
- |
|
20 |
280,7 |
251.2 |
246,2 |
- |
|
10 |
276,3 |
247.5 |
_ |
_ |
Литература
I. Истомин В.А. Предупреждение и ликвидация газовых гидратов в системах сбора и промысловой обработки газа и нефти. М., 1990. 214 с. 78
2» Истомин В.А., Квон В.Г., Бурмистров А.Г., Лакеев В.П. Инструкция по расчету оптимального расхода ингибиторов гидрато-образования. М.: ВНИКГАЗ, 1987. 72 с.
3. Sloan E.D., Jr. Clathrate Hydrates of Natural Gases//
Chem. Industries ser. 1990, V.39. New-York, Marcel dekker inc.,
1990.
664 p.
4, Истомин В.А.э Якушев B.C., Карпюк В.В.
Аналитический
библиографический указатель литературы по
газовым гидратам
(1983-1987). М.: ВНИИГАЗ, 1988. 246 с.
5. Ш Y,, Guo Т.-М.
Prediction of Hydrate formation for
systems, containing methanol//Chem. Eng. Soi. 1990, V.45. N 4,
P.893-900.
6, Ступин Д.Ю., Маширов Ю.Г., Ким Н.А., Плющев Д.В. Иссле
дование ингибирующего действия продукта
прямого окисления ме
тана кислородом воздуха на образование
гидрата//Природные и тех
ногенные газовые гидраты (Под
ред.А.И.Гриценко, В.А.Истомина).
М.: ВНИИГАЗ, 1990,
Л.А.Корбачков, В.Л.Палесик (Коми филиал ВНИИГАЗа)
ЭНЕРГЕТИЧЕСКАЯ МОДЕЛЬ ДЛЯ РАСЧЕТА ПОВЕРХНОСТНОГО НАТЯЖЕНИЯ ВОДЫ
Поверхностное натяжение (поверхностная энергия) - весьма важная характеристика поверхности раздела фаз, обусловливающая эффекты многих физических явлений, в том числе и эффект понижения температуры замерзания воды в дисперсных средах; к которым относятся, например, буровые растворы, цементный камень, грунты и т.п. Однако до настоящего времени величину поверхностного натяжения жидкости находят преимущественно инструментально, и поэтому конкретную зависимость поверхностного натяжения от температуры можно получить только экспериментальным путем / I /„
В настоящей работе показано, что величину поверхностного натяжения воды можно выразить через энергетические характеристики молекулярной связи и тем самым установить конкретный вид температурной зависимости поверхностного натяжения воды в терминах энергетической модели /2, 3/.
79
Удельную поверхностную энергию воды в предельном случае можно интерпретировать как отношение нескомпенсированной части минимальной энергии молекулярной связи к площади поверхности, занимаемой одной молекулой / 4 /.
В рамках энергетической модели минимальная энергия связи молекулы вода определяет величину теплоты парообразования /2,3/.
![]() +
+
2 V Го
а радиус молекулы воды
выражается через среднее значение энер
гии связи _.//
R = А ■ £ " ,
(2)
где tmin - минимальная энергия связи молекулы воды, эВ; Г -теплота парообразования, эВ/молекула; Го - теплота парообразования в тройной точке, эВ/молекула; с ~ безразмерный коэффициент теплоемкости воды /2, 3/; к - постоянная Больцмана, эВ/К; °1 = Т - 10 - температура, К ( Т - текущая температура, К; То - температура тройной точки, К); R - радиус молекулы, м; Д - коэффициент перевода размерностей, численно равный 9,7596 Ю"11 (СИ); £ - средняя энергия связи молекулы воды, рассчитываемая по уравнению /2/
z
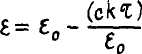
(3)
где £0 - энергия при граничных условиях модели, эВ, вычисляемая по значению плотности воды в тройной точке
Ь°~ 8 \ М ) ' . (4)
где рд - плотность воды в тройной точке, кг/м3; М - молярная масса, кг/кмоль; В - коэффициент перевода размерностей численно равный 3,5300836 10"^ (СИ).
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.