![]()
|
Д Т
2 -
i -
![]() 250
250
260
265
Т. К
|
Н- = F (Т) |
Рис. 3, Зависимость
для смеси Ш 2, Конценграция иетанола - 50 иао.% давление - 97 кгс/см
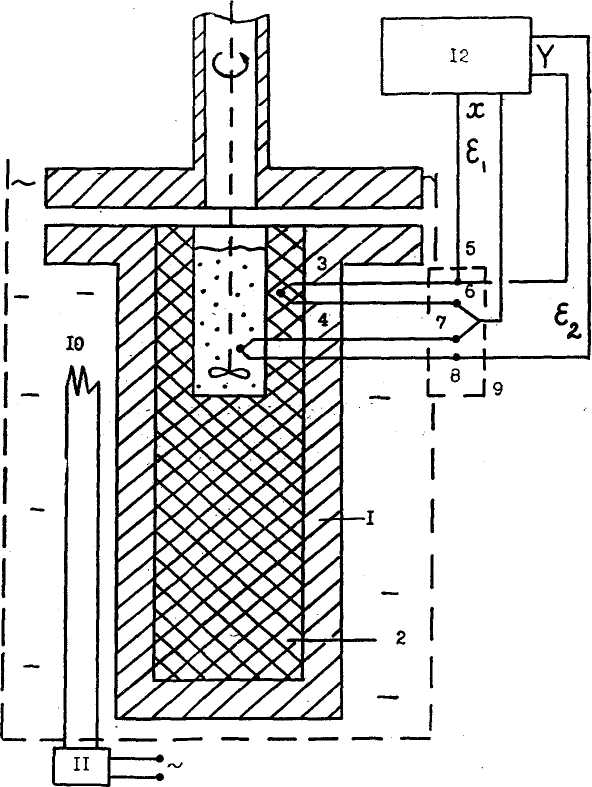
Рис.4. Модификация реактора установки для термографических исследований в гидратообразующей системе
75
нагрева на элемент 10, добивались равномерного роста температуры термостата во времени (о(т/о("theorist). В ходе нагрева при
помощи вентиля тонкой регулировки избыток давления, возникающий вследствие теплового расширения газа, периодически сбрасывали, приводя значение давления к заданному. При таком нагреве и при отсутствии фазовых или химических превращений в исследуемом растворе значение ДТ будет определяться лишь скоростью нагрева системы (инерционность системы принимается постоянной), т.е. температура раствора всегда будет на постоянную величину ниже температуры стенки стакана. Если же в ходе нагрева в растворе (в нашем случае содержащем частица газового гидрата) будут происходить какие-либо процессы, сопровождающиеся эндо- и экаоэффек-тами, величина ДТ в области температур, при которых эти превращения происходят, будет меняться. При этом на кривой aT=Fj(T)
(кривая ДТА) будут проявляться особенности (пики, либо перегибы), характеризующие эти процессы. На рис.5 представлена типичная кривая ДТА, которая получена нами для гидратов, выращенных из газовых смесей.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Сравненке кривых ДТА для калибровочного состава газа № 3 с данными Нгэ и Робинсона (см. / 3 /, р.374), показывает, что равновесная температура гидратообразования при заданных давлениях на кривых ДТА соответствует максимуму экзотермического пика, непосредственно предшествующего большому пику эндотермического разложения гидрата. Поэтому температура, отвечающая экзотермическому пику, и интерпретировалась авторами как искомая температура разложения гидрата. Однако физическая природа обнаруженного экзотермического процесса (предплавления) остается не вполне ясной и требует дополнительного изучения. Как наглядно видно из рис.5, на термограммах фиксируется еще один эндотермический процесс, предшествующий основному процессу разложения гидрата структуры П. Этот пик авторами интерпретируется как процесс разложения метастабильного гидрата структуры I, который образуется наряду с основным количеством гидрата структуры П при наработке гидрата.
В таблице представлены полученные данные по условиям разложения гидрата для смеси газов № I. Аналогичная информация полу-
76
йТ,К
ИГ1-!
|
|
275
т
280
285
290
295 Т,К
Рис.5. Термограмма разложения газового гидрата смеси № 2 (для дистиллированной воды и давления 40 кгс/см )
77
чена также и для смеси газов № 2, но в последнем случае процесс гидратообразования осложняется частичной конденсацией пропана. Обсувдение этих результатов будет выполнено в отдельном сообщении. Данные таблицы по условиям гидратообразования из чистой воды хорошо согласуются с разработанной ранее методикой инженерного расчета равновесных параметров гидратообразования / 1,2 /. В диапазоне давлений 6*13 МПа полученные данные описываются следующей зависимостью для величины ДТ - снижения температуры гидратообразования:
, I00-w
Д Т = - 68СП ---------------------- •
100 - 0.4375 Х^
где \ас - мае!? метанола в растворе. Тогда как интерполяция
данных Нгэ и Робинсона по условиям гидратообразования чистого метана в воднометанольных средах приводит к коэффициенту 77 перед логарифмом / 2 /. Таким образом, при переходе от метана к газовым смесям содержащим, помимо метана, также этан и пропан, ингибируицая способность растворов метанола несколько снижается. Поэтому требуется корректировка некоторых зависимостей, используемых в инструкции / 2 /.
Условия гидратообразования трехкомпонентной газовой смеси: 90,20 об.$ СН4, 6,95 % C^g и 2,85 % CgHg в присутствии водо-метанольного раствора
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.