Основны положения теории радикального цепного механизма реакции термического распада У.В Теория РАЙСА
1. Первичный распад молекулы идет по связи –С–С– с образованием двух радикалов
![]()
2. Относительно устойчивыми радикалами являются H•, СН3•, С2Н5•. Продолжительность жизни метильного и этильного радикалов составляет соответственно 0,006 и 0,002 с. Более крупные радикалы неустойчивы и подвергаются распаду. Распад крупных радикалов происходит по связи –С–С–, находящейся в β-положении относительно атома углерода, имеющего неспаренный электрон.
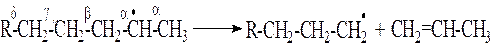
Это обусловлено тем, что наличие свободного электрона вызывает усиление связей α за счет электронного взаимодействия его с электронами соседних углеродных атомов и ослабление связей β.
Распад крупных радикалов протекает до образования устойчивого радикала. При этом в результате распада образуется радикал с меньшим числом углеродных атомов и непредельный углеводород.
3. Радикалы, взаимодействуя с нейтральной молекулой, могут отрывать от нее атом водорода
![]()
Легкость отрыва атома водорода от молекулы углерода уменьшается в ряду:
третичный атом углерода > вторичный > первичный.
Скорости отрыва атома водорода от первичного, вторичного и третичного атомов углерода при 600 0С соотносятся как 1:2:10.
4. Радикалы могут взаимодействовать между собой с образованием нейтральной молекулы углерода. Новая связь С-С образуется за счет двух неспаренных электронов, имеющихся у радикалов.
![]()
![]()
механизма термического крекинг н-бутана.
1 стадия. Зарождение цепной реакции. На этой стадии происходит распад молекул н-бутана на радикалы
![]()
![]()
![]()
2 стадия. Развитие цепной реакции. На этой стадии образовавшиеся на первой стадии радикалы реагируют с новыми молекулами н-бутана.

или
![]()
![]()
или
![]()
3. стадия. Распад радикалов. Образовавшиеся на 2й
стадии радикалы подвергаются распаду по ![]() -правилу.
-правилу.
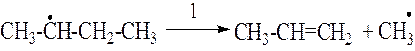
![]()
4 стадия. Передача цепи. Образовавшиеся на 3й стадии радикалы взаимодействуют с новыми молекулами н-бутана и превращаются в нейтральные молекулы (метан и этан соответственно) – коечные продукты распада исходного углеводорода наряду с С2Н4 и С3Н6, образовавшимися на 3й стадии.
![]()
![]()
Бутильные радикалы далее подвергаются распаду (см. 3ю стадию)и таким образом происходит цепная реакция распада.
5 стадия. Обрыв цепной реакции. Он заключается во взаимодействии радикалов между собой и прекращении цепной реакции.
![]()
![]()
![]()
Очевидно, что распад н-бутана может протекать по двум направлениям
![]()
![]()
Относительную вероятность протекания реакции по тому или иному направлению можно определить по формуле
![]()
где К – относительная скорость отрыва водорода от первичного или вторичного атома углерода;
nH – число атомов водорода у атома углерода, от которого происходит отрыв водородного атома;
nС – число равноценных атомов углерода в молекуле.
Вероятность первой реакции равна 2*2*2=8.
![]()
Вероятность второй реакции равна 1*3*2=6.
![]()
Таким образом, 14 молекул н-бутана распадаются на 8 молекул С3Н6, 8 молекул СН4, 6 молекул С2Н4 и 6 молекул С2Н6. На основании этих данных рассчитывается теоретический состав продуктов распада н-бутана и сравнивается с экспериментальными данными. Теория радикально-цепного механизма крекинга была проверена также на примере распада н-гексана, изооктанов, н-октана и других алканов и во всех случаях было показано хорошее соответствие теории и эксперимента по составу продуктов реакции при небольших глубинах превращений исходных углеводородов.
Превращение различных углеводородов при термическом крекинге.Рассмотрим поведение углеводородов различных классов под воздействием высоких температур.Парафиновые углеводороды. Для парафинов характерен распад на низкомолекулярные углеводороды. Продуктами первичного распада парафинового углеводорода являются парафин и олефин.
![]()
Распад алканов происходит преимущественно по середине цепи, так как центральные связи С–С являются наименее прочными. Так, в н-октане энергия разрыва связей составляет, кДж/моль
![]()
Низкомолекулярные алканы наряду с распадом подвергаются в значительной степени реакциям дегидрирования с образованием соответствующих олефинов
![]()
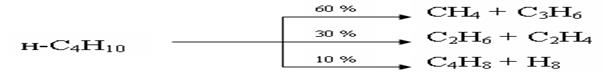
По мере увеличения молекулярной массы углеводорода вероятность реакций дегидрирования снижается. Так, пропан при 600 0С в равной степени превращается по двум направлениям

Нормальный бутан в тех же условиях подвергается дегидрированию уже в значительно меньшей степени
Нафтеновые углеводороды. Термическая устойчивость незамещенных нафтеновых углеводородов значительно выше, чем парафинов. Лишь в жестких условиях крекинга возможен распад кольца нафтенового углеводорода с образованием олефинов или очень неустойчивых бирадикалов, которые в свою очередь распадаются с образованием олефинов:
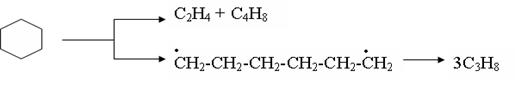
При жестких условиях протекает дегидрирование моноциклических нафтенов до соответствующих ароматических углеводородов. Эта реакция идет через стадию образования непредельных углеводородов
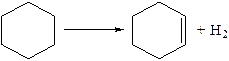
![]()
![]()
Наиболее вероятным направлением крекинга алкилированных нафтеновых углеводородов является разрыв связей С–С в боковой цепи.
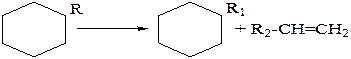
При ужесточении режима может происходить полное деалкилирование углеводорода
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.