2.13. В соответствии с распределением Больцмана концентрация молекул водорода и углекислого газа меняется с высотой по формуле
ni = ni0 exp(–migh/RT),
где i = 1, 2 (соответственно для H2 с m1 = 2 и CO2 с m2 = 44).
Изменение относительного содержания H2 и CO2 с высотой будет определяться равенством
n1/n2 = n10/n20 exp((m2 – m1)gh/RT),
откуда
![]()
2.14. В лабораторной системе отсчета газ в центрифуге вращается как единое целое, стало быть, имеется центростремительное ускорение, т. е. система не находится в механическом равновесии и к ней нельзя применить распределение Больцмана. В системе же отсчета, связанной с центрифугой, объект исследования находится в равновесии, и к нему можно применить указанное распределение. Но в этой системе отсчета на частицы действует центробежная сила. Соответствующая потенциальная энергия частицы равна
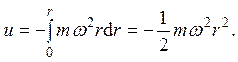
Распределение Больцмана с учетом цилиндрической симметрии имеет вид
![]()
где l – высота барабана центрифуги. Выражение для статистической суммы получается из условия нормировки распределения
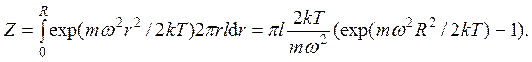
В результате для концентрации частиц получается формула
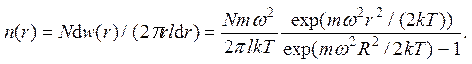
Из формулы следует, что концентрация тяжелых частиц у боковой стенки центрифуги относительно выше, что используется для разделения смесей. Концентрация частиц у боковой стенки центрифуги равна
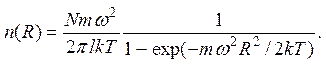
Соответствующее отношение концентраций молекул D2 и H2 будет
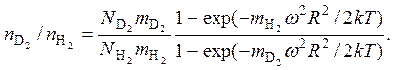
С учетом того, что масса молекулы дейтерия в два раза тяжелее и начальная пропорция изотопов водорода D2 и H2 равна b, при отборе смеси у боковой стенки центрифуги можно увеличить долю дейтерия
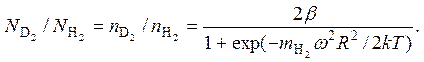
Максимальное соотношение компонент в смеси равно
![]()
2.15. Пусть для определенности спектр энергии системы непрерывный. Распределение Гиббса для нее будет
dw = 1/Z×exp(–e/kT)dG/hf,
где dG – элемент объема фазового пространства, hf – объем этого пространства, отвечающий одному состоянию системы (h – постоянная Планка, f – число степеней свободы системы). Статистическая сумма Z находится из условия нормировки
![]()
Интегрирование выполняется по всему доступному объему фазового пространства.
По определению, средняя энергии системы равна
![]()
Использование техники дифференцирования по параметру позволяет получить искомую формулу:
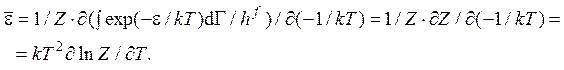
Эта формула остается в силе, если спектр энергии дискретный. Она применима также в случаях распределений Максвелла и Больцмана.
2.16. Распределение газа по высоте hопределяется барометрической формулой: n(h) = n0ехр(–mgh/kT), где n0 – концентрация молекул в вершине воронки (при h = 0). Величины N и n0 связаны соотношением:
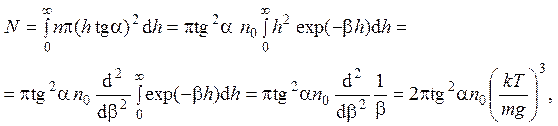 где b = mg/kT.
где b = mg/kT.
Отсюда
n0 = N/(2ptg2a)∙(mg/kT)3, p0 = n0kT = N(mg)3/(kT)2/(2ptg2a).
Средняя потенциальная энергия молекулы
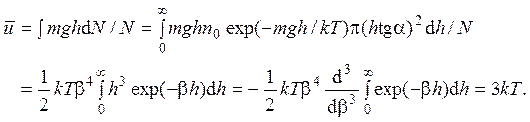
2.17. Полная энергия атома равна сумме кинетической и потенциальной энергий: e = mv2/2 + u(r). Кинетическая энергия определяется скоростью теплового движения атома, потенциальная зависит только от его положения. Поэтому статистическая сумма распадается на два множителя: Z = Z1Z2, где Z1 соответствует распределению Максвелла, а Z2 – распределению Больцмана. Таким образом, средняя энергия теплового движения атома равна ЗkТ/2. Чтобы найти среднее значение потенциальной энергии, надо вычислить статистическую сумму
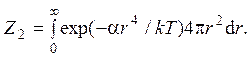
Здесь в качестве элемента объема рассматривается сферический слой радиуса r и толщины dr. Интеграл в элементарных функциях не вычисляется, но зависимость его от температуры может быть найдена. Для этого следует сделать замену переменных t = (α/kT)1/4r. Тогда
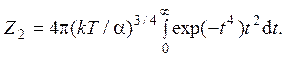
Интеграл в атом выражении для Z2 является константой. Поэтому
ln Z2 = const + ¾ lnT.
Средняя потенциальная анергия атома равна
![]()
Среднее значение энергии атома
![]()
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.