В этом случае система A¢может находиться только в пяти равновероятных доступных состояниях. Они перечислены в таблице.
|
№ |
s1 |
s2 |
s3 |
s¢1 |
s¢2 |
M |
M¢ |
|
1 |
1 |
1 |
1 |
1 |
–1 |
3m0 |
0 |
|
2 |
1 |
1 |
1 |
–1 |
1 |
3m0 |
0 |
|
3 |
1 |
–1 |
–1 |
1 |
1 |
–m0 |
4m0 |
|
4 |
–1 |
1 |
–1 |
1 |
1 |
–m0 |
4m0 |
|
5 |
–1 |
–1 |
1 |
1 |
1 |
–m0 |
4m0 |
И в этих пяти состояниях магнитный момент первой системы может принимать только два значения: 3m0 и –m0. Вероятности этих двух значений равны w(3m0) = 2/5 и w(–m0) = 3/5 (число состояний с заданным магнитным моментом подсистемы поделить на число состояний, которые удовлетворяют фиксированному значению полной энергии системы, в данном случае E0 = –3m0 B).
. Среднее значение магнитного момента этой подсистемы равно
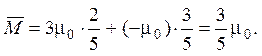
2.4. Энергия полной системы A + A¢ равна
E0 = 3m0B – 4m0B = –m0B.
При установлении равновесия полная система может находиться в любом из семи доступных состояний: (– – –, + +), (– + +, – +), (+ – +, – +), (+ + –, – +), (– + +, + –), (+ – +, + –), (+ + –, + –). Только в одном из них магнитный момент системы A равен –3m0, в остальных шести он равен +m0. Возможные значения этого момента не реализуются. Таким образом,
w(–3m0) = 1/7, w(+m0) = 6/7, w(+3m0) = w(–m0) = 0.
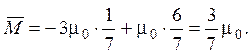
2.5. Наиболее вероятная скорость атомов идеального газа равна
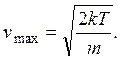
По условию задачи n×vmax = const. Откуда следует, что ![]() или (с учетом того, что концентрация
атомов n = NА/V, где NА – число Авогадро, V – молярный объем),
или (с учетом того, что концентрация
атомов n = NА/V, где NА – число Авогадро, V – молярный объем), ![]() (A – постоянная). Для идеального
газа теплоемкость
(A – постоянная). Для идеального
газа теплоемкость
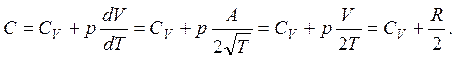
2.6. Распределение Максвелла для идеального газа в общем случае имеет вид
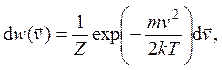
где ![]() –
элемент объема пространства скоростей, Z – статистический интеграл
(нормировочная постоянная).
–
элемент объема пространства скоростей, Z – статистический интеграл
(нормировочная постоянная).
Для двумерного газа распределение принимает вид
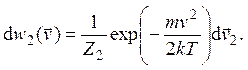
Здесь ![]() –
элемент объема двумерного пространства скоростей, а Z2 – статистический интеграл
двумерного газа, его значение находится из условия нормировки:
–
элемент объема двумерного пространства скоростей, а Z2 – статистический интеграл
двумерного газа, его значение находится из условия нормировки:
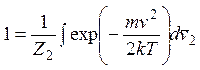 ,
,
где интегрирование проводится по всему доступному частице газа пространству скоростей.
Если в этом двумерном пространстве ввести декартовые координаты vx и vy, то элемент объема равен
![]()
Подставляя значение ![]() в распределение, а также вычисляя
нормировочную постоянную, получаем
в распределение, а также вычисляя
нормировочную постоянную, получаем
dw(vx, vy) = m/2pkT×exp(– m(vx2 + vy2)/2kT) dvx dvy,
Якобиан перехода от декартовых координат к полярным равен единице, поэтому, чтобы получить распределение в полярных координатах, достаточно в полученном распределении для декартовой системы координат выразить элемент объема в пространстве скоростей через переменные полярной системы координат. В полярных координатах v и j элемент объема в пространстве скоростей равен
![]()
Отсюда получаем:
dw(v, j) = ( m/kT×exp(– mv2/2kT) v dv×) (dj/2p) = dw(v)dw(j),
где dw(v) и dw(j) – нормированные распределения по модулю скорости vи углу j:
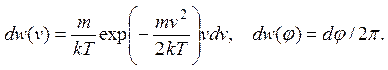
Средняя энергия молекулы идеального двумерного газа равна
![]() =
m
=
m![]() /2 =
/2 = 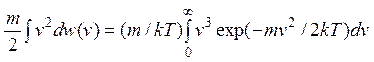 = kT.
= kT.
Замечание. Интеграл может быть вычислен методом дифференцирования по параметру:
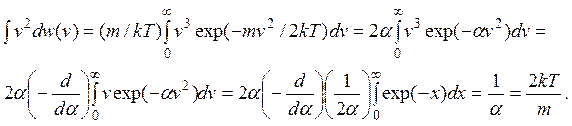
2.7. Распределение Максвелла для идеального двумерного газа имеет вид
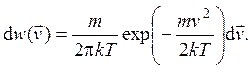
Здесь ![]() –
элемент объема двумерного пространства скоростей. Если в этом пространстве
выразить элемент объема через полярные координаты и проинтегрировать по угловой
координате, получим распределение по величине скорости (см. задачу 2.6)
–
элемент объема двумерного пространства скоростей. Если в этом пространстве
выразить элемент объема через полярные координаты и проинтегрировать по угловой
координате, получим распределение по величине скорости (см. задачу 2.6)
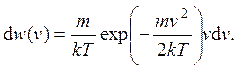
Средняя скорость теплового движения молекул двумерного газа равна
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.