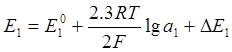
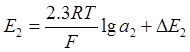 ,
,
где ![]() - стандартный потенциал никеля,
- стандартный потенциал никеля, ![]() и
и ![]() -
активности ионов никеля и водорода соответственно,
-
активности ионов никеля и водорода соответственно, ![]() и
и ![]() - перенапряжение разрядов ионов никеля и
водорода.
- перенапряжение разрядов ионов никеля и
водорода.
Соотношение скоростей процесса разряда ионов никеля и водорода зависит от факторов, влияющих на равновесный потенциал и перенапряжение (состав электролита, температура, катодная плотность тока). При pН = 3¸5 никель выделяется на катоде. При повышении катодной плотности тока, доля тока, идущая на выделение никеля, увеличивается. С повышением температуры выход по току никеля увеличивается. Для активации никелевых анодов вводят ион Cl- в виде NiCl2×6H2O, NaCl, или KCl.
Для получения блестящих покрытий вводят выравнивающие добавки. Для устранения питтинга вводят поверхностно-активные вещества, например, моющие средства. Электролит для никелирования чувствителен к загрязняющим примесям металлов, таких как свинца, или меди.
Электрохимическое цинкование.
Стандартный потенциал цинка, равный –0.76 В, более отрицателен, чем у железа, чугуна, или стали. В паре с ними цинк является анодом и защищает металл электрохимически. Защитные свойства цинка сохраняются и в случае пористости или частичного повреждения покрытия. Скорость разрушения цинкового покрытия в жестких условиях характеризующихся наличием в среде диоксида серы, диоксида углерода и в присутствии хлорид-ионов составляет 6¸20 мкм в год. Для повышения защитных свойств цинкового покрытия оцинкованные детали хроматируют в растворах солей хромовой кислоты, или фосфатируют. Для цинкования применяют два основных типа электролитов:
Простые кислые электролиты характеризуются высоким выходом по току и низкой катодной поляризацией. Цинк из электролита выделяется на катоде в результате разряда простых гидратированных ионов по реакции: Zn+2 + 2e ® Zn.
Добавки органических веществ (декстрин, гуммиарабик) способствуют повышению катодной поляризации и образованию более качественных мелкокристаллических светлых осадков. Для увеличения электропроводности электролита в него вводят сульфат натрия и поддерживается pН в пределах 4¸4.5. При pН > 5 на катоде образуется гидроксид цинка, снижающий качество катодного осадка. При pН < 4 уменьшается выход по току на катоде цинка вследствие выделения водорода. Для стабилизации кислотности в сернокислый электролит вводят буферную добавку Al2(SO4)3.
Al2(SO4)3 + 6H2O Û 2Al(OH)3 + 3H2SO4
Это позволяет поддерживать кислотность электролита на требуемом уровне. Вредными примесями в кислых электролитах являются все соли электроположительных металлов: медь, свинец, серебро, олово и др., нитраты этих металлов, скипидар, ацетон. В их присутствии образуется губчатое покрытие. Примеси железа в электролите делают осадки цинка пятнистыми и неравномерными, так как в покрытие включается гидроксид железа. Кислые электролиты не ядовиты и экономичны, но покрытие получается неравномерным. Кислые электролиты применяются для цинкования изделий простой конфигурации: листы, проволка, ленты, и т.д. Для получения блестящего покрытия вводятся блескообразующие добавки.
В щелочно-цианидных электролитах цинк находится в виде комплексных анионов [Zn(CN)4]-2 и [Zn(OH)4]-2 и цинк выделяется на катоде при восстановлении адсорбированного комплексного аниона: [Zn(CN)4]-2 + 2e ® Zn + 4CN-.
Цианидные электролиты обеспечивают мелкозернистую структуру катодных осадков. С повышением концентрации цианида натрия увеличивается рассеивающая способность электролита, но снижается выход по току цинка. С увеличением концентрации едкого натра расширяется интервал рабочих плотностей тока, повышается выход по току, но рассеивающая способность уменьшается и возможно образование синильной кислоты. Цианидные электролиты ядовиты, имеют низкий выход по току цинка и неустойчивый состав. Тем не менее, цианидные электролиты находят широкое применение в автомобильной промышленности. Цинкатные электролиты не ядовиты. В них цинк содержится в виде комплексного аниона [Zn(OH)4]-2. Они имеют хорошую рассеивающую способность и электропроводность. С увеличением плотности тока в таких электролитах значительно уменьшается выход по току. Их применяют для нанесения покрытий в барабанных и колокольных ваннах.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.