11. Ароматичность фурана. Правило Хюккеля (4n+2).
12. Ароматичность тиофена. Резонансные структуры тиофена.
13. Ароматичность пиррола. Эффект сопряжения.
14. Как изменяется ароматический характер в ряду фуран, пиррол, тиофен?
15. Укажите, как происходит передача электронных влияний в молекуле H2FC─ СН=СН ─C(О)H при взаимодействии её с Н+.
16.
Укажите как происходит передача
электронных влияний в молекуле ![]() при взаимодействии её с Cl+.
при взаимодействии её с Cl+.
17.
Укажите как происходит передача
электронных влияний в молекуле 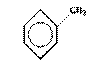 при взаимодействии её с Cl-.
при взаимодействии её с Cl-.
18. Укажите как происходит
передача электронных влияний в молекуле 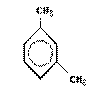 при взаимодействии её с NO2+.
при взаимодействии её с NO2+.
19. Cравните силу оснований (H3C)3N и (F3C)3N.
20. На основании электронных эффектов объясните почему
гексаметилдисилициламид лития {[(H3C)3Si─N ─Si(CH3)3]- Li+ } является особенно сильным основанием.
Тема 6.ТИПЫ ОРГАНИЧЕСКИХ РЕАКЦИЙ.
Задания к теме 6.
1. Укажите типы реакций в цепочке превращений: .
t0,Pt +HBr +KOH
[2 – метилпентан] ¾¾® А ¾¾® Б ¾¾® В
(-H2) (H2O2) (спирт.)
2. Укажите типы реакций в цепочке превращений:
+KOH Br2 Mg
[2,3 – дихлор – 2,3 - диметилпентан] ¾¾® А ¾¾® Б ¾¾®
HCl Na (спирт.)
® В ¾¾® Г ¾¾® ?
3. Укажите типы реакций в цепочке превращений:
+HBr KOH
[2- метилбутен –1] ¾® A ¾¾® Б.
4.Укажите, чем различаются типы реакций присоединения и синтеза.
5. Укажите, чем различаются типы реакций отщепления и расщепления.
6. Укажите строение молекулы органических соединений, которые не могут участвовать в реакциях присоединения?
7. Укажите тип реакции: (n+1)НООС─С6Н4─СООН + nНО─СН2─СН2─ОН
→ НООС─С6Н4─(С(О)─О─СН2─СН2─О─(О)С─С6Н4─)n─СООН + n Н2О
8. Укажите тип реакции Вюрца.
9. Укажите в чем различие реакций типа изомеризации и замещения.
10. В чем различие реакций полимеризации и поликонденсации?
Тема 7. МЕХАНИЗМЫ ОРГАНИЧЕСКИХ РЕАКЦИЙ. (При изучении механизмов реакций в органической химии фундаментальным понятием является электроотрицательность элементов см. Приложение 1).
Задания к теме 7.
1. Объясните причину образования побочных продуктов в свободно – радикальных реакциях. Укажите основные стадии свободно – радикального механизма.
2.Укажите, в чем различие при разрыве связей в реакциях отщепления и расщепления.
3. Укажите, какие связи разрываются в реакциях замещения. Какие варианты разрыва связей при этом возможны. Какие механизмы реакций замещения возможны?
4. Укажите механизм реакции взаимодействия бензола с NO2+ c указанием всех переходных состояний.
5. Приведите пример разрыва связей в молекуле органического соединения с образованием карбокатиона.
6. Приведите пример разрыва связей в молекуле органического соединения с образованием карбаниона.
7. Какие атакующие частицы называются электрофильными? Приведите пять примеров электрофильных частиц.
8. Укажите как положительные
индуктивные эффекты (+I) влияют на стабилизацию электрофильной частицы в
ряду:{(Н3C)3![]() C+} ; { (Н3C)2
CH+}; {
Н3C─ CH2+};{ Н3C+}.
C+} ; { (Н3C)2
CH+}; {
Н3C─ CH2+};{ Н3C+}.
9. Укажите гибридизацию третичного атома углерода и строение карбкатиона {R3C+}.
10. Приведите пример реакции электрофильного замещения.
11. Приведите пример реакции электрофильного присоединения.
12. Какие атакующие частицы называются нуклеофильными? Приведите пять примеров нуклеофильных частиц.
13. Приведите пример реакции нуклеофильного замещения.
14. Приведите пример реакции нуклеофильного присоединения.
15. Укажите гибридизацию и строение насыщенного карбаниона {R3C─}, способы образования свободных радикалов.
16. Укажите, как отрицательные индуктивные эффекты влияют на стабилизацию нуклеофильной частицы. Сравните устойчивость карбанионов:
{(F3C)3![]() C─} и {H3
C─} и {H3![]() C─}.
C─}.
17. Металлоорганические производные представляют собой нуклеофильные реагенты, успешно используемые в органической химии для проведения реакций конденсации. Укажите как влияет электроотрицательность металла на реакционную способность таких нуклеофильных реагентов( см. приложение –таблица электроотрицательностей): R ─ K; R ─ Na; R ─ Li; R ─ Mg─; R ─ Zn─, где R─ - карбанион.
18. Какие частицы называются свободными радикалами? Укажите гибридизацию и строение радикала {R` R``R```C•}.
19. Приведите три примера различных способов образования свободных радикалов.
20. Какие типы реакций могут идти по свободно – радикальному механизму?
Варианты заданий к разделу 1.
Таблица 1
|
Вариант № |
Тема 1 № |
Тема 2 № |
Тема 2 № |
Тема 4 № |
Тема 5 № |
Тема 6 № |
Тема 7 № |
|
1 |
5; 12; 21 |
4; 15 |
3; 10 а) |
2 |
2; 15 |
2; 8 |
5; 17 |
|
2 |
2; 8; 23 |
1; 19 |
6; 10 б) |
7 |
5; 14 |
1; 10 |
3; 16 |
|
3 |
6; 11; 22 |
2; 13 |
2; 10 в) |
6 |
3; 17 |
4; 9 |
1; 19 |
|
4 |
7; 10; 24 |
5; 12 |
5; 10 и) |
10 |
8; 11 |
3; 6 |
2; 14 |
|
5 |
4; 9; 25 |
7; 14 |
8; 10 ж) |
4 |
4; 19 |
2; 7 |
4; 15 |
|
6 |
3; 11; 22 |
3; 17 |
7; 10 е) |
5 |
7; 16 |
1; 6 |
7; 18 |
|
7 |
1; 7; 23 |
8; 20 |
1; 10 д) |
8 |
9; 20 |
2; 9 |
6; 11 |
|
8 |
3; 12; 25 |
6; 11 |
4; 10 г) |
9 |
1; 18 |
3; 10 |
8; 20 |
|
9 |
5; 10; 26 |
9; 16 |
5; 10 з) |
1 |
10; 13 |
4; 7 |
10; 13 |
|
10 |
4; 11; 24 |
10; 18 |
8; 10 к) |
3 |
6; 12 |
5; 8 |
9; 12 |
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.