|
Галогеноводородная соль образует с H2SO4 галогеноводород, который, взаимодействуя с эфиром серной кислоты. Дает галогеналкил:
NaCl + H2SO4 → HCl + NaHSO4;
Галоидные соединения фосфора при действии спирта легко замещают их гидроксильную группу на галоген :
3R – OH + PCl3 → 3R – Cl + H3PO3;
R – OH + PCl5→ R – Cl + HCl + POCl3.
При взаимодействии PCl3 с первичными спиртами в качестве побочного прдукта образуется сложный эфир фосфористой кислоты :
3R – OH + PCl3 → (RO)3P + HCl
Для реакции со спиртами можно брать не готовые PBr3и PJ3, а вводить в реакционную смесь отдельно фосфор и галоген. В этом случае со спиртами реагируют галогениды фосфора в момент их образования:
2P + 3I2 = 2PI3; 3R – OH + PI3 → 3R – I + H3PO3
Хлорпроизводные с высоким выходом получают при действии на спирты хлористого тионила SOCl2 :
R – OH + SOCl2 → R – Cl + HCl↑ + SO2↑.
В этом случае образуются газообразные HCl и SO2, которые легко отделяются от галогеналкана.
Считают, что спирт сначала взаимодействует с SOCl2 и образует алкилхлорсульфит (1), который затем образует внутреннюю ионную пару (II), а она далее разлагается с сохранением конфигурации:
![]()
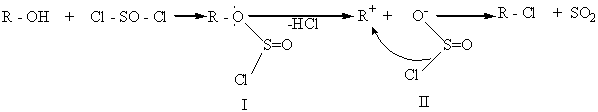
Спирты вступают в реакцию с минеральными и органическими кислотами. Продуктами такого взаимодействия являются соответствующие сложные эфиры. Если в реакцию со спиртами вступает многоосновная кислота, то в зависимости от соотношения кислоты и спирта, введенных в реакцию, могут образовываться или кислые, или сложные эфиры:
|
|
|
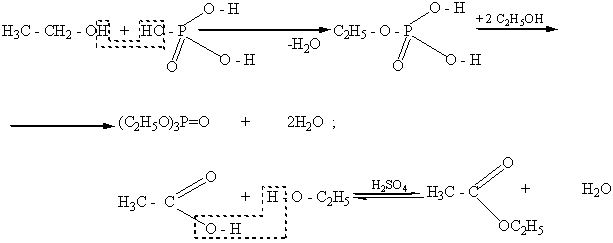
Дегидратация спиртов может осуществляется в двух направлениях: внутримолекулярно и межмолекулярно. Направление дегидратации зависит от природы спирта и условий проведения реакции.
При внутримолекулярной дегидратации спирта образуется ненасыщенный этиленовый углеводород, в результате межмолекулярной дегидратации – простой эфир. Так, при нагревании спиртов с такими водоотнимающими веществами, как концентрированная H2SO4, H3PO4, безводная щавелевая кислота, оксид алюминия и т.д., образуются ненасыщенные соединения этиленового ряда.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.