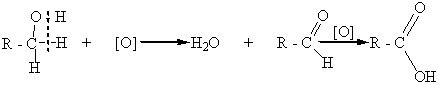
альдегид карбоновая кислота
Окисление спиртов хромовой смесью сопровождается изменением оранжево-красного окрашивания реакционной смеси (ионы Cr2O72-) на зеленое (ионы Cr3+):
![]()
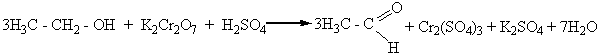
Первичные спирты можно также окислить в альдегиды мелко раздробленной медью. Нагретой до 280-300оС. В этих условиях от молекулы спирта отщепляются два атома водорода и в молекуле органического вещества, которая при этом образуется, появляется двойная связь углерод – кислород (>C=O). Такое превращение спиртов называется дегидрированием:
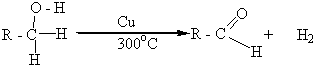
Вторичные спирты при окислении, а также при дегидрировании, превращаются в кетоны:
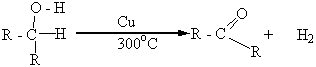
Например, втор-пропиловый спирт в этих условиях превращается в кетон, который называют ацетоном:
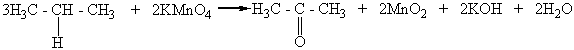
Диметилкетон
(ацетон)
Третичные спирты окисляются достаточно трудно с одновременным разрывом углеродной цепи их молекул и образования смеси карбоновых кислот и кетонов. Такое окисление этих спиртов связано с тем, что в условиях реакции окисления они дегидратируются и превращаются в этиленовые углеводороды, которые в присутствии сильного окислителя окисляются с разрывом молекулы по месту двойной С=C - связи.
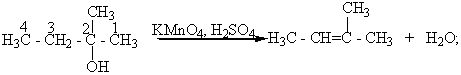
2- Метилбутанол-2 2-Метилбутен-2.
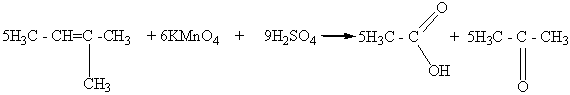
Уксусная Диемтилкетон
кислота (ацетон)
Таким образом, по продуктам окисления спиртов можно сделать вывод о строении спиртов.
Спирты можно отличить от других классов органических веществ по цветной реакции с оксидом хрома (IV) в среде серной кислоты. Хромовый ангидрид CrO3 в водном растворе H2SO4 окисляет первичные и вторичные спирты, на протяжении приблизительно двух секунд прозрачный оранжевый раствор реакционной смеси становится голубовато-зеленым и мутнеет. Третичные спирты этой реакции не дают.
Для того, чтобы установить, каким является данный спирт – первичным, вторичным или третичным пользуются пробой Лукаса. Эта проба основана на разной реакционной способности спиртов относительно галогеноводородов. Спирты, молекулы которых содержат не больше шести углеродных атомов, растворяются в реактиве Лукаса, который представляет собой смесь концентрированной соляной кислоты и хлорида цинка. При растворении спирта в этом реактиве образуются соответствующие алкилхлориды, раствор мутнеет, поскольку алкилхлориды в реактиве Лукаса не ратсворяются. Время, необходимое для появления помутнения реактива Лукаса, является мерой реакционной способности спирта. Третичные спирты реагируют с реактивом Лукаса сразу же, вторичные спирты – на протяжении 5 минут, а первичные спирты прикомнатной температуре с этим реактивом почти не взаимодействуют.
![]() Этиловый спирт и спирты
общей формулы взаимодействуют
Этиловый спирт и спирты
общей формулы взаимодействуют
в щелочной среде с иодом и образуют иодоформ CHJ3 (иодоформная реакция). По способности давать иодоформную реакцию можно отличить данные спирты от других спиртов:
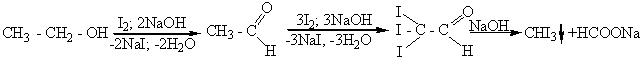
этиловый уксусный трииодуксусный иодоформ имеет
спирт альдегид альдегид неприятный запах
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.