Пассивность металла зависит как от внутренних (состав, структура и состояние поверхности металла), так и от внешних факторов (состав и концентрация электролита, температура, движение раствора, наложение постоянного тока и т.д.).
О большей или меньшей склонности металла к пассивированию можно судить по пассивирующей концентрации окислителя или пассивирующей анодной плотности тока.
Пассивное состояние металла может в большей или меньшей степени сохраняться и после изменения внешних пассивирующих условий. При изменении внешних условий металл может вновь перейти в активное состояние, т.е. депассивироваться или активироваться.
Депассивирующие факторы
Депассивирующими или активирующими факторами, нарушающими пассивное состояние металлов, или затрудняющими наступление пассивности являются:
а) восстановители - H2, Na2SO3, Na2S2O3;
б) катодная поляризация (восстановление поверхности металла в электролите постоянным электрическим током) от внешнего источника постоянного электрического тока или при работе пассивного металла в качестве катода в паре с другим металлом, выполняющим роль анода;
в) некоторые ионы: H+, галоидные ионы Cl-, Br-, J-, SO4-2 и др.;
г) повышение температуры;
д) механические нарушения пассивной поверхности металла, например образование царапин. Царапина служит анодом и катодно поляризует пассивную поверхность.
Значительное замедление анодного процесса растворения металлов в пассивном состоянии происходит в результате изменений заряда и свойств поверхности металлов, вызванных образованием на ней адсорбционных, фазовых или адсорбционно-фазовых плёнок.
При большом повышении анодного потенциала, или окислительно-восстановительного потенциала среды у некоторых металлов, например Cr, Mo, Fe, Ni и др., наблюдается нарушение пассивности – перепассивация (или транспассивность), которое приводит к возрастанию скорости коррозии. Она объясняется изменением характера анодного процесса – образуются ионы металла внешней валентности, дающие растворимые или неустойчивые соединения (железо и хром образуют ионы FeO4-2 и CrO4-2), что приводит к нарушению пассивного состояния и скорость растворения металла увеличивается.
Поляризационные кривые.
Потенциостатические анодные поляризационные кривые для стали имеют следующие характерные области и точки:
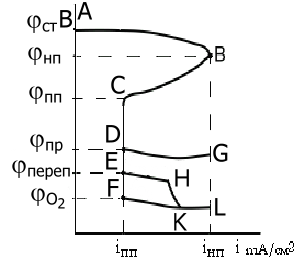
AB – область растворения стали в активном состоянии;
BC – область пассивации стали (область частично-пассивного или активно-пассивного состояния);
CDEF – область полной пассивации стали;
DG – область точечной коррозии стали;
EH – область перепассивации стали;
FKL – область разряда ионов гидроксида с выделением кислорода;
jСТ - стационарный потенциал;
jН.П. и i Н.П. - потенциал и плотность тока начала пассивации;
jП.П. и i П.П. - потенциал и плотность полной пассивации стали;
jПР - потенциал начала точечной коррозии;
jпереп - потенциал начала перепассивации стали;
![]() - потенциал начала
образования O2 из ионов гидроксида.
- потенциал начала
образования O2 из ионов гидроксида.
На стали, не склонной в условиях опыта к точечной коррозии и перепассивации, измеряется кривая ABCDEFKL (на железе, низколегированной и углеродистых сталях в разбавленной серной кислоте при комнатной температуре). При склонности стали к точечной коррозии, измеряемая кривая имеет вид ABCDG (на хромистых и хромоникелевых сталях в растворах, содержащих Cl-).
При отсутствии точечной коррозии, по возможности перепассивации могут быть получены кривые вида ABCDEH или ABCDEHKL (на хромистых и хромоникелевых сталях в H2SO4; на железе и углеродистых сталях в щелочных средах).
Чем меньше i Н.П и более отрицательные значения jН.П. и jП.П., тем легче сталь пассивируется. Стойкость стали в пассивном состоянии характеризуется величиной i Н.П., чем меньше эта плотность тока, тем устойчивее сталь. Склонность стали к точечной коррозии характеризуется значением потенциала пробивания jПР Чем отрицательнее значение jПР, тем больше склонность стали к точечной коррозии. О склонности хромоникелевых сталей к МКК. (межкристаллитной коррозии) можно судить по увеличению после провоцирующего отпуска этих сталей тока пассивации i Н.П. и сдвигу в положительную сторону потенциала полной пассивации jП.П.. При усилении процесса МКК наблюдается увеличение плотности тока полной пассивации i П.П..
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.