Эти методы – бесспорные лидеры по количеству созданных установок.
Са(ОН)2 суспензия – известковый,
СаСО3 суспензия – известняковый.
1-ый более щелочной, более эффективный, но более дорогой:
2Са(ОН)2 + 2SO2 ® ¯2CaSO3 × 0,5H2O + H2O
2-ой менее реакционный, но более дешевый:
CaСO3 + SO2 + 0,5H2O ® ¯CaSO3 × 0,5H2O + CO2
Скорость образования CaSO3 × 0,5H2O (осадок) зависит от рН среды, температуры, времени контакта, избытка поглотителя.
После стадии абсорбции суспензии отработанные выводятся из оборота и в специальных ёмкостях при 100 °С подвергаются обработке кислородом воздуха.
CaSO3 × 0,5H2O + 0,5О2 + 1,5H2O ® 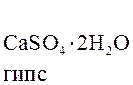
Преимущества:
- дешевизна
- малое потребление энергии
- высокая эффективность при низком гидродинамическом сопротивлении системы в целом и малом соотношении абсорбент – газ.
Недостатки:
- большое образование твёрдых отходов
- потребление » 2 % мощности котла
- выделение углекислого газа.
К новинкам последнего времени с целью улучшения технологии:
· введение стадии предочистки с помощью гидроциклонов и скрубберов Вентури;
· Количественное окисление сульфита кальция в гипс и его использование с строительной индустрии.
· Замыкание жидкофазного цикла для уменьшения потребления воды.
· Использование добавок к абсорбенту для повышения начальной очистки от SOx: ПАВ, карбоновые кислоты, соли магния.
Мокро-сухой нециклический процесс.
Является совершенствованием процесса, описанного выше.
В основу метода положено поглощение диоксида серы из дымовых газов испаряющимися каплями известкового раствора.
Дымовые газы очищаются от золы и поступают в реактор, куда подается тонкораспыленная смесь раствора извести. Сухие продукты реакции отделяют в пылезолоуловителе. Уловленную смесь CaCO3 и CaSO4 термическим методом перерабатывают в сульфат кальция, который является строительным материалом.
Преимущества:
- получение сухого твёрдого продукта
- отсутствие сточных вод
- высокая степень испарения реагента
- низкое гидравлическое сопротивление.
Недостатки:
- использование высококачественной извести.
Метод аммиачной абсорбции SOx.
Используют водные растворы аммиака NH4OH (25%).
Абсорбции триоксида серы может быть описана следующими уравнениями:
SO2 + 2NH3 + H2O ® (NH4)2SO3
SO3 + 2NH3 + H2O ® (NH4)2SO4
(NH4)2SO3 + 0,5O2 ® (NH4)2SO4
Процесс протекает с образованием полезного продукта сульфата аммония (NH4)2SO4 (минеральное удобрение). Используют адсорбер диаметром 4м и высотой 35 м, степень очистки: 90%.
Недостатки:
- повышенный расход поглотителя.
- происходит потери аммиака
- высокие капитальные затраты.
Большого распространения этот процесс не получил.
Регенерационные методы сероочистки.
Эти методы мало используются промышленностью, но более перспективны, т.к. позволяют получить такие вещества, как H2SO4, S, SO2.
Магнезитовый циклический процесс.
Суть метода: использование в качестве сорбента оксида и гидроксида магния, цинка, бария и др.
SO2 + Mg(OH)2 ® ¯MgSO3 + H2O
1) Отфильтрованный MgSO3 подвергают термической обработке:
MgSO3 ![]() SO2 + MgO
SO2 + MgO
MgO + H2O ® Mg(OH)2
SO2 можно каталитически окислить на ванадиевом катализаторе и получить SO3
2) MgSO3 приводят в контакт с углеродом в термических печах:
MgSO3+С+ H2O ![]() MgO+СO2+
H2S
MgO+СO2+
H2S
4H2S+ 2SO2®3S2¯+ H2O (процесс Клауса)
Преимущества:
- гибкость метода
- получение H2S, S, SO2
Недостатки:
- дороговизна
- коррозия газоходов.
- потребность в электроэнергии 6-7% от мощности котла
- потери MgO (0,07 моль/моль уловленного SO2 )
Аммиачно-циклический процесс.
Процесс разработан в начале 60-х годов.
(NH4)2SO3
+ SO2 + H2O ![]() 2NH4H SO3
2NH4H SO3
Реакция протекает с выделением тепла, т.е. тепло надо отводить.
При температуре до 350С реакция проходит в прямом направлении, степень очистки от SO2 до 90%, при кипячении реакция идет в обратном направлении с регенерацией поглотителя и выделением SO2(г)
Этот процесс позволяет получить 100% SO2
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.