1. М(газ) - ? Використовуючи наслідок з закону Авогадро, складаємо пропорцію:
1,714 г газу займають 600 мл;
х г газу займають 22400 мл;
х = (22400 . 1,714)/600 = 63,9 г
Оскільки 22400 мл це – мольний об’єм газу, М(газ) = 63,9 г/моль.
Відповідь: М(газ) = 63,9 г/моль
в) Визначення молярної маси газу за законом Менделєєва - Клапейрона.
Приклад 4. Визначити молярну масу бензолу, якщо маса 600 мл його пари при 87°С і тиску 83,2 кПа дорівнює 1,30 г.
Розв’язок:
Виразимо всі дані в одиницях СІ:
Р = 8,32 104 Па; Т = 273 + 87 = 300К; V = 6 10-4 м3; m = 1,3 10-3 кг.
1. М(С6Н6) - ?
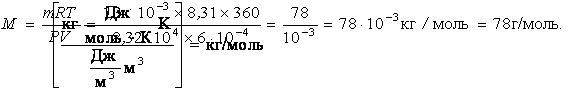 |
Відповідь: молярна маса бензолу дорівнює 78 г/моль.
1. Дати визначення ¢¢моль речовини¢¢.
2. Сформулювати закон Авогадро та наслідки з нього.
3. Дати визначення ¢¢відносна густина одного газу за другим¢¢.
4. Записати рівняння стану ідеального газу і розрахувати значення R у різних одиницях.
5. Записати способи визначення молярної маси газу.
6. Визначити кількість молей і кількість атомів, які містяться у: 32 г кисню, 14 г азоту, 8 г кисню, 10 г водню.
7. Скільки молей атомів Нітрогену містять 1 моль нітратної кислоти; 2 моль амоніаку; 2 моль амоній нітрату?
8. Які необхідні експериментальні дані, щоб визначити молярну масу газу всіма відомими вам способами?
9. Визначити густину за воднем газової суміші, яка складається з 70 % карбон (ІІ) оксиду та 30 % карбон (ІV) оксиду за об’ємом.
10. За нормальних умов 500 мл газу мають масу 1,806 г. Визначити його відносну густину за повітрям і молярну масу.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.