но это означает, что нулю равен косинус угла между векторами напряжённости и элементарного перемещения. Следовательно, угол между ними должен быть равен 90о.
|
|
Поскольку перемещение, по усло-вию, совершается вдоль эквипотен-циальной поверхности, то и угол между силовой линией, пересекаю-щей эквипотенциальную поверхность, и поверхностью – прямой.
Отсюда следует важное свойство эквипотенциальной поверхности: эк-випотенциальная поверхность всегда перпендикулярна пересекающим её силовым линиям электро-статического поля.
Таким образом, построив линию, перпендикулярную всем пересекаемым эквипотенциалям, мы получим силовую линию.
Густота полученных таким образом силовых линий будет выше там, где гуще расположены эквипотенциали. Следова-тельно, по густоте эквипотенциалей можно судить о напряжён-ности поля – чем гуще эквипотенциали, тем выше напряжённость поля.
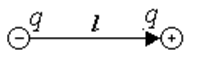 Электрический диполь –
это система из двух одинаковых по величине и противо-положных по знаку зарядов,
находящихся на расстоянии l друг от друга.
Электрический диполь –
это система из двух одинаковых по величине и противо-положных по знаку зарядов,
находящихся на расстоянии l друг от друга.
Основной характеристикой диполя является дипольный момент, который по определению равен
р = ql,
где р – дипольный момент, q – величина зарядов диполя, l – плечо диполя (вектор, соединяющий заряды и направленный от отрицательного заряда к положительному). Размерность диполь-ного электрического момента [p] = Кл.м.
Как следует из определения, дипольный момент есть векторная величина, прямо пропорциональная величине зарядов диполя и расстоянию между ними. Дипольный момент направлен так же, как и плечо диполя – от отрицательного заряда к положительному.
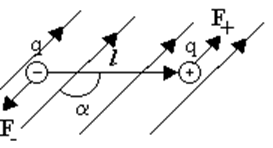 Если поместить диполь
в однородное электрическое поле напряжённостью Е, то на заряды
диполя действуют одинаковые по величине и противоположные по направлению силы |F+|
= |F-| = qE.
Если поместить диполь
в однородное электрическое поле напряжённостью Е, то на заряды
диполя действуют одинаковые по величине и противоположные по направлению силы |F+|
= |F-| = qE.
Равнодействующая этих сил равна нулю, поэтому диполь не будет двигаться поступательно. Но эти силы создают момент пары сил, который стремится повернуть диполь так, чтобы дипольный момент был параллелен силовым линиям.
Величина момента пары сил, действующего на диполь, равна
![]() ,
,
где р –дипольный момент.
Диэлектриками принято называть вещества, не проводящие электрический ток.
В молекулах диэлектрика, как и в молекулах других веществ, суммарный положительный заряд ядер всех атомов, образующих молекулу, равен суммарному отрицательному заряду всех электронов.
В общем случае заряд всех
ядер молекулы можно заменить одним точечным положительным зарядом. Величина
этого заряда равна сумме зарядов ядер всех атомов молекулы, а положение
совпадает с положением центра ![]() “тяжести” положительных
зарядов молекулы.
“тяжести” положительных
зарядов молекулы.
В свою очередь, суммарный отрицательный заряд электронов молекулы можно заменить одним точечным отрицательным зарядом, расположенном в центре «тяжести» зарядов электронов.
Если центры «тяжести» положительным и отрицательных зарядов находятся на расстоянии l друг от друга, то молекулу можно считать диполем с плечом l.
В некоторых диэлектриках молекулы симметричны (напри-мер, Н2, О2, N2). У таких молекул центры тяжести положительных и отрицательных зарядов совпадают.
В диэлектриках второго типа
молекулы состоят из противо-положных по знаку ионов (например, NaCl, KCl,
KBr).
В отсутствие внешнего электрического поля центры “тяжести” положительных и
отрицательных зарядов ионных молекул в кристалле диэлектрика совпадают.
В отсутствие внешнего электрического поля молекулы диэлектриков первого и второго типа не обладают собственным дипольным моментом, они неполярны. Поэтому диэлектрики, состоящие из таких молекул, называют неполярными.
В диэлектриках, состоящих из несимметричных молекул (например, NH3, CO, H2O), центры “тяжести” отрицательных и положительных зарядов не совпадают. Следовательно, такие молекулы обладают собственным дипольным моментом. Поэтому их называют полярными.
Несмотря на наличие дипольных моментов у всех молекул такого диэлектрика, диэлектрик в целом в отсутствие внешнего электрического поля дипольным моментом не обладает, так как вследствие теплового движения полярные молекулы ориен-тированы хаотично и их суммарный дипольный момент равен нулю.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.