Данные о кинетике окисления сульфидных цинковых концентратов, необходимы для правильного расчета печей. Они должны учитываться при осуществлении обжига в кипящем слое. Кинетические закономерности процесса взаимодействия газа с твердым веществом определяются кристаллохимическими превращениями и диффузией газа между реакционной поверхностью и внешней газовой средой, а также условиями теплообмена.
Проход газов через твердое тело подчиняется закону диффузии и определяется вторым законом Фика:
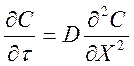 , (1.6.)
, (1.6.)
где С – концентрация газов;
![]() - время реагирования;
- время реагирования;
D – числовой коэффициент;
Х – путь газов.
В зависимости от сочетания диффузионного процесса и химического взаимодействия реагирующих веществ возможен тот или иной режим протекания реакции. При малой скорости химической реакции по сравнению со скоростью диффузии ход процесса определяется законами химической кинетики. Если процесс лимитируется проходом газов, то наблюдаемая скорость реакции определяется скоростью диффузии. Если скорость химической реакции и диффузии газа соизмеримы, то процесс приобретает промежуточный характер, на него оказывают влияние и кинетические и диффузионные факторы. При малых скоростях газового потока скорость процесса может тормозиться внешней диффузией. Последняя обусловлена тем, что вокруг зерна материала образуется слой, обогащенный газообразными продуктами реакции.
Характеристикой граничного условия
перехода из кинетической области в диффузионную служит температура воспламенения
сульфидов ![]() . В ряду сульфидов, наиболее типичных для
цинкового концентрата,
. В ряду сульфидов, наиболее типичных для
цинкового концентрата, ![]() возрастает в последовательности
СuFeS2, FeS, PbS, ZnS. В атмосфере О2 при скоростях
нагрева 30
возрастает в последовательности
СuFeS2, FeS, PbS, ZnS. В атмосфере О2 при скоростях
нагрева 30![]() /мин увеличение крупности фракций от (-30
+10) до (-500 +200) мкм повышает
/мин увеличение крупности фракций от (-30
+10) до (-500 +200) мкм повышает ![]() следующим образом: для
ZnS от 625 до 680
следующим образом: для
ZnS от 625 до 680![]() ; для PbS от 545 до 607
; для PbS от 545 до 607![]() ; для FeS от 375 до 480
; для FeS от 375 до 480![]() ; для СuFeS2 от 330 до 420
; для СuFeS2 от 330 до 420![]() . Для сфалерита (Zn, Fe)S величина
. Для сфалерита (Zn, Fe)S величина ![]() растет с увеличением содержания
изоморфного железа: 500, 507, 520 и 545
растет с увеличением содержания
изоморфного железа: 500, 507, 520 и 545![]() соответственно
при его содержании 2; 4; 6 и 8%.
соответственно
при его содержании 2; 4; 6 и 8%.
Поскольку окисление сульфидов протекает в далеких от равновесия условиях и поэтому необратимо, то скорость процесса равна скорости прямой реакции в кинетической области или скорости диффузии О2 в диффузионной области.
Степень вторичного сульфатообразования в процессе обжига МеS имеет максимум при изменении температуры. Это обусловлено тем, что повышение температуры, с одной стороны, ускоряет реакцию МеО + SО3 = МеSО4, а с другой стороны, снижает долю SО3 в газовой фазе из-за сдвига влево равновесия реакции 2 SО2 + О2 = 2 SО3. Чем выше термическая стойкость сульфатов и выше концентрация оксидов серы в газовой фазе, тем больше температура максимума сульфатизации при обжиге и выше степень сульфатизации.
Кинетически термическую стойкость
сульфатов можно характеризовать температурой начала заметного разложения ![]() , которая зависит от ряда условий. Величины
, которая зависит от ряда условий. Величины
![]() для технологически важных компонентов
цинковых концентратов образуют следующий ряд,
для технологически важных компонентов
цинковых концентратов образуют следующий ряд, ![]() : Fe2(SО4)3
530; СuSО4 620; ZnSО4 670; СuО
: Fe2(SО4)3
530; СuSО4 620; ZnSО4 670; СuО![]() 720;
720; ![]() 760; CdSО4 840; PbSО4 860.
760; CdSО4 840; PbSО4 860.
В зависимости от условий обжига
цинковых концентратов и содержания в газовой фазе SО2 и О2 температура,
соответствующая максимуму сульфатизации цинка, лежит в пределах 750 - 850![]() [1].
[1].
Слой шихты, пронизываемый восходящим потоком воздуха,
может находиться в двух качественно различных стационарных состояниях:
спокойном и псевдоожиженном. При скорости газового потока ![]() ниже некоторой критической величины
ниже некоторой критической величины ![]() зерна в слое неподвижны, объем
межзеренного пространства постоянен. При
зерна в слое неподвижны, объем
межзеренного пространства постоянен. При ![]() <
<![]() рост
рост ![]() сопровождается
пропорциональным увеличением давления дутья. При достижении
сопровождается
пропорциональным увеличением давления дутья. При достижении ![]() =
= ![]() давление
дутья становится равным давлению спокойного слоя шихты на подину. Зерна в слое
теряют контакт, слой расширяется, переходит в псевдоожиженное состояние и
напоминает кипящую жидкость. При дальнейшем росте
давление
дутья становится равным давлению спокойного слоя шихты на подину. Зерна в слое
теряют контакт, слой расширяется, переходит в псевдоожиженное состояние и
напоминает кипящую жидкость. При дальнейшем росте ![]() слой
начинает расширяться и интенсивность движения зерен увеличивается при
практически постоянном давлении дутья до тех пор, когда
слой
начинает расширяться и интенсивность движения зерен увеличивается при
практически постоянном давлении дутья до тех пор, когда ![]() станет
больше второй критической величины
станет
больше второй критической величины ![]() , при которой давление
дутья начинает быть существенно больше давления спокойного слоя на подину. При
, при которой давление
дутья начинает быть существенно больше давления спокойного слоя на подину. При ![]() >
> ![]() зерна
выносятся из слоя. Скорость
зерна
выносятся из слоя. Скорость ![]() называется скоростью
начала псевдоожижения, а
называется скоростью
начала псевдоожижения, а ![]() - скоростью начала
уноса.
- скоростью начала
уноса.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.