ОКИСЛЕНИЕ ЛИГНИНА
По сравнению с углеводами лигнин более легко окисляется. что объясняется его фенольной природой, В органической химии метод окисления часто используют для определения строения органических соединений. Однако применительно к лигнину этот метод долгое время не давал решающих результатов. Чаще всего при окислении лигнина как в нейтральной, так и в кислой и щелочной средах получаются продукты глубокого окисления, такие как уксусная, щавелевая, муравьиная- кислоты и даже угольная кислота. Однако эти продукты не позволяют охарактеризовать строение лигнина.
В случае окисления лигнина кислородом в щелочной среде при нагревании до 200—250.°С под давлением был получен ряд ароматических кислот: бензойная С6Н3СООН, фталевая C6H4(COOH)2 тримеллитовая C6H3(COOH)3, пиромеллитовая C6H2(COOH)4, бензолпентакарбоновая C6H(COOH)5 и меллитовая C6(COOH)6. Эти опыты послужили одним из первых доказательств ароматической природы лигнина.
Позднее было показано, что лигнин реагирует с кислородом в щелочной среде и при температуре 20° С. С повышением температуры и давления кислорода реакция окисления усиливается, Эти исследования легли в основу разработки способа кислородно-щелочной отбелки целлюлозы.
Большое значение в химии лигнина приобрел метод мягкого окисления лигнина нитробензолом в щелочной среде с получением из хвойного лигнина ванилина, а из лиственного лигнина—ванилина и сиреневого альдегида. Ванилин получается только из «незамещенных» единиц. Наряду с ванилином получается и ванилиновая кислота.
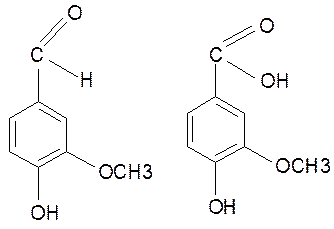
Замещенные единицы (в 5-м положении) дают продукты другого строения:
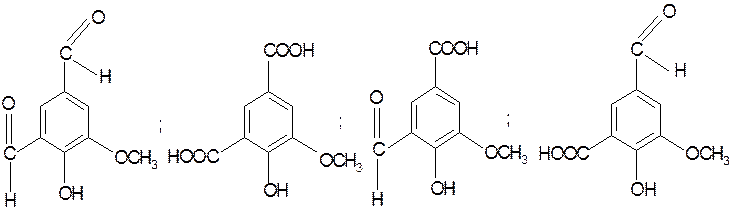
Из дифенильных структур при этом образуются продукты следующего строения:
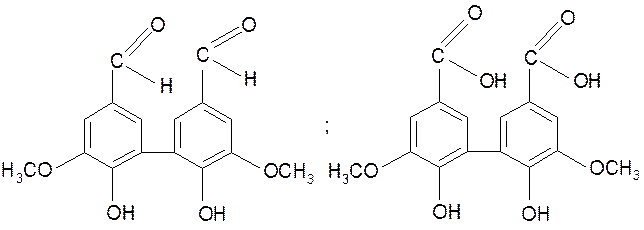
Подобные продукты можно получать и при окислениилигнина другими окислителями, например Cu(OH)2 в присутствии NаОН. Кроме того, при таком окислении удалось получить 1 продукты окисления, сохраняющие пропановую боковую цепь. Так, например, была получена феруловая кислота
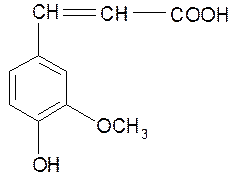
Для изучения строения сложных органических соединений содержащих двойные связи, часто применяют реакцию озонирования. Таким способом было установлено, например, строение природного каучука. Однако при действии озона на лигнин долгое время получали лишь продукты глубокого распада. Как показал Д. В. Тищенко, при озонировании лигнина в безводной среде (в этилацетате) из различных лигнинов получаются триозониды с выходами, соответствующими теоретическому в соответствии со схемой реакции
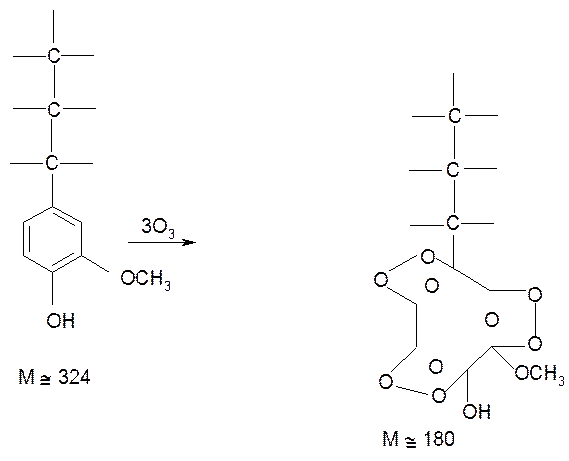
Теоретический выход триозонида 180%. Практически выход триозонидов составлял около 176—180%. При разложении триозонида с последующим окислением перманганатом калия были получены соответствующие продукты и в том числе (СООН)2 с выходом близким к теоретическому. Это доказывает, что лигнин полностью построен из фенилпропановых единиц.
Реакция окисления лигнина имеет большое значение при отбелке технических целлюлоз. На легкой окисляемости лигнина основаны косвенные методы определения содержания остаточного лигнина в технических целлюлозах (например, по хлорным и перманганатным числам).
СПЛАВЛЕНИЕ ЛИГНИНА СО ЩЕЛОЧЬЮ ПО ФРЕЙДЕНБЕРГУ
Метод сплавления лигнина со щелочью (по Фрейденбергу) применяют для определения в лигнине замещенных (конденсированных) и незамещенных (неконденсированных) единиц. Этот метод заключается в обработке лигнина 60—70%-ным КОН при температуре 170—210.° С с последующим метилированием фенольных продуктов деструкции (для предохранения их от дальнейшего разложения) и окислением перманганатом калия. При сплавлении со щелочью происходит разрыв как кислородных, так и углерод-углеродных связей, за исключением связи между α -углеродом пропановой цепочки и ароматическим кольцом. Из незамещенных фенилпропановых единиц хвойного лигнина 'при такой
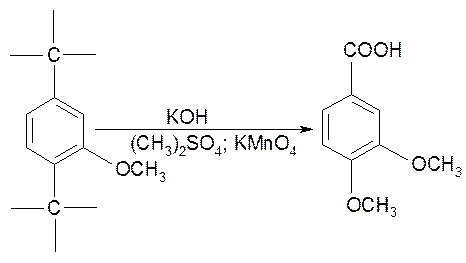
Из замещенных единиц с углеродной связью β -5' получается изогемипиновая кислота
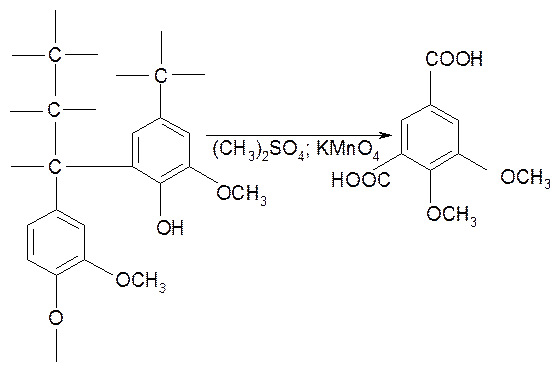
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.