Хлорлигнин может применяться как понизитель вязкости глинистых растворов при бурении нефтяных скважин и в ряде других областей народного хозяйства.
При действии хлора на влажную древесину или хлорной воды на. древесину или техническую целлюлозу идет реакция замещения с выделением хлористого водорода (хлорирование);
RH + CI2 = RCI + HCI
Одновременно идут и окислительные процессы под действием хлорноватистой кислоты, образующейся по обратимой реакции
CI2
+ H2O![]() HCI + HCIO
HCI + HCIO
HCIO = HCI + O
Соляная кислота в системе хлор — вода полностью диссоциирована на ионы:
HCI
![]() H+
+ CI-
H+
+ CI-
Хлорноватистая кислота диссоциирована сравнительно мало:
HCIO
![]() H+ + CIO-
H+ + CIO-
Действие хлора в присутствии воды определяется рН среды, в зависимости от которого в системе хлор—вода будут преобладать молекулярный хлор CI2, хлорноватистая кислота НСI или ионы гипохлорита СI. В сильно кислой среде при рН ниже 2 преобладает молекулярный хлор и основной реакцией лигнина является хлорирование. При рН от 4 до 6 в системе преобладает кислота, и поэтому окисление лигнина проявляется особенно сильно в результате распада хлорноватистой кислоты:
HCIO = HCI + O
При рН 6—8 присутствуют и НС10 и ионы СЮ" и в щелочной среде преобладающими будут уже ионы гипохлорита — более слабый окислитель:
HCIO + OH- ![]() H2O + CIO-
H2O + CIO-
Механизм хлорирования лигнина изучали Гибберт с сотрудниками, Сарканен, а также Фрейдснберг, Шорыгина и Др. При воздействии хлора на лигнин можно заметить две стадии реакции. Сначала идет быстрая реакция главным образом замещения хлором водорода в ароматическом кольце. Вторая стадия, более медленная, соответствует окислительным реакциям, протекающим с разрушением боковых цепей и расщеплением молекул лигнина.
Процесс хлорирования является очень сложным. Предполагают, что во время его двух стадий происходят реакции нескольких типов.
1. Быстрая реакция электрофнльного замещения хлором водорода в ароматическом кольце, причем в фенольных единицах (содержащих свободный фенольный гидроксил) замещение происходит главным образом в 5-м положении, а в нефенольных единицах (с этерифицированным фенольным гидроксилом) — в 6-м положении.
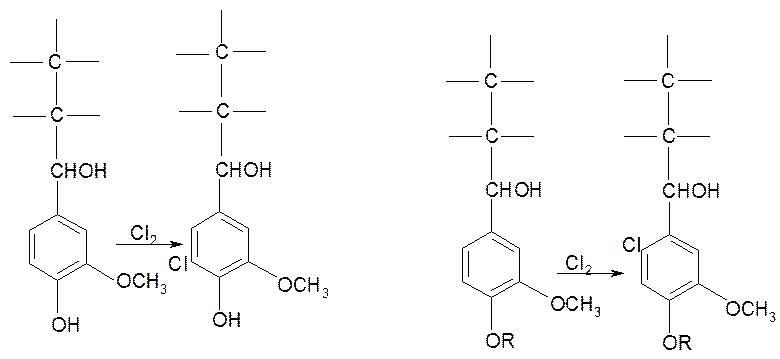 2.
Деметилирование лигнина, которое идет медленнее реакции замещения и в основном
после него (причем, чем ниже рН, тем быстрее идет эта реакция)
2.
Деметилирование лигнина, которое идет медленнее реакции замещения и в основном
после него (причем, чем ниже рН, тем быстрее идет эта реакция)
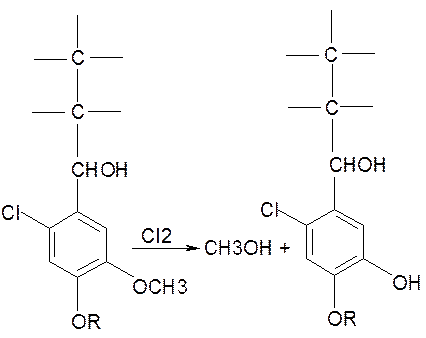
3. Гидролитическое расщепление простых эфирных связей между структурными единицами лигнина с получением низкомолекулярных фрагментов.
4.Электрофильное вытеснение боковой цепи хлором.
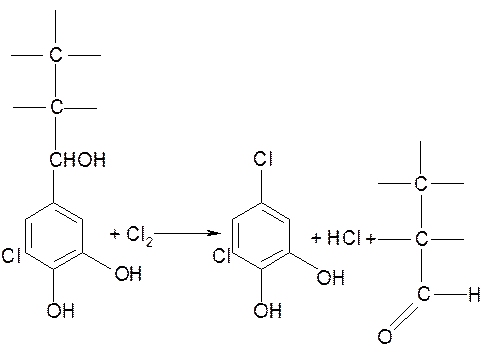
Этой реакции способствует наличие группировок n-оксибензилового спирта.
5. Окисление группировок пирокатехина, образующихся при деметилировании, с превращением их в о-хиноны
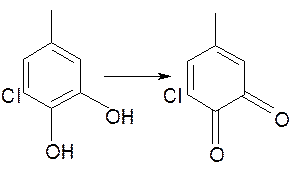
Эти соединения под действием других окислителей (например, при гипохлоритной отбелке) разрушаются до алифатических карбоновых кислот.
Реакции гидролиза простых эфирных связей и вытеснения боковых цепей значительно уменьшают размер молекул лигнина, превращая его в продукты, растворимые в щелочи или даже в воде. Получающиеся при этом хлорлигнины представляют собой сложные смеси разных продуктов.
3.2. ДЕЙСТВИЕ НА ЛИГНИН АЗОТНОЙ КИСЛОТЫ
Азотная кислота нашла применение для делигнификации древесины с целью получения целлюлозы. Разработан так называемый азотно-щелочной способ варки целлюлозы, заключающийся в обработке древесины разбавленной азотной кислотой HNO3 (2—7%-ной) при температуре близкой к температуре кипения. Лигнин нитруется и окисляется азотной кислотой, а гемицеллюлозы гидролизуются. Продукты распада лигнина удаляются при обработке разбавленным раствором NаОН при нагревании. Особенно хорошие результаты этот способ дает при варке лиственной древесины и однолетних растений.
На делигнификации азотной кислотой основан также способ количественного определения содержания целлюлозы в древесине (способ Кюршнера).
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.