Гідроліз аніонів та катіонів. Якщо у природному розчині присутні міцні катіоногенні елементи (Na+, К+) і іони слабких кислот (HCO3- CO32- H2S-, H3BO3- та ін.), відбувається гідроліз цих аніонів, який супроводжується розкладом води і зв’язуванням іона H+ у слабкодисоціюючу сполуку. В результаті активність іона OH- стає більшою за активність H+:
CO32- + H2O ↔ HCO3- + OH-;
HCO3- + H2O = HCO3- + OH-;
HS- + H2O = H2S + OH- і т.п.
Константа гідролізу має вигляд:
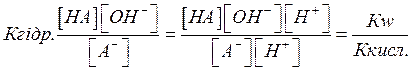
Звідси важливий висновок: збільшення рН у реакціях гідролізу аніонів є зворотно пропорційним константі дисоціації кислоти.
Збільшення рН в результаті гідролізу аніонів інтенсифікується зі зростанням температури.
Оскільки у звичайних умовах серед аніонів слабких кислот у підземних водах превалює іон HCO3-, то вважається, що лужності підземні води набувають в основному за рахунок гідролізу карбонатних іонів. Але насправді лужність підземних вод обумовлюється дією багатьох аніонів слабких кислот у тому числі і органічних. У зв’язку з цим можна виділити карбонатну, силікатну, боратну, сульфатну і та ін. лужність.
Не меншого значення для формування кислотно-лужних умов підземних вод має гідроліз катіонів. Якщо у природному розчині присутні аніони сильних кислот та елементи з малими значеннями коефіцієнтів розчинності гідроокисів або комплексних гідроксосполук (елементи – комплексоутворювачі), відбувається гідроліз катіона, в результаті якого спостерігається зв’язування іонів OH- (a H+ стає більшим за a ОН- і зменшується рН розчину). Зменшення рН у реакціях гідролізу катіонів тим сильніше, чим меншою є константа дисоціації основи. За здатністю знижувати рН підземних вод катіони розташовуються у порядку збільшення їхніх кислотних властивостей, які, у свою чергу, відповідають збільшенню електронегативності елементів:
Na+<Ca+<Mg2+<Fe2+<Al3+<Fe3+.
Інтенсивність зниження рН при гідролізі катіонів збільшується зі збільшенням температури підземних вод.
В підземних водах гідроліз катіонів супроводжується відповідними реакціями гідролізу аніонів і тому кисневі значення рН у сукупності цих реакцій залежать від співвідношення констант дисоціацій кислот і основ, що утворюються внаслідок хімічних реакцій.
Значення рН підземних вод змінюються від < 0 до 12,5, але у більшості випадків складають 6 ÷ 8,5.
Мінімальними значеннями рН (<0-2) характеризуються термальні води і конденсати вулканічних газів районів сучасного магматизму. Кислі води (рН<2-5) розповсюджені в зонах окислення сульфідних родовищ, що вміщують дисульфіди (пірит та ін.). Кисла реакція середовища (рН до 4 і менше) також може бути характерною для висококонцентрованих (М<400 г/дм3) розсолів Cl-Ca-Na, Cl-Ca-Mg, Cl-Ca-Mg-Na складу, які залягають у негативних структурах земної кори, що вміщують галогенні формації.
У земній корі широко розповсюдженими є підземні води з лужною реакцією. Типовими у цьому відношенні є азотні термальні води, які формуються у масивах кристалічних порід HCO3–Na складу при дуже високому вмісті (H3SO4-). Підземні води з високим значеннями рН (>8) також утворюються у осадових породах краєвих прогинів і міжгірських западин (особливо альпійського віку). Вони мають Cl-HCO3-Na або Cl-Na склад, вміщують високі концентрації HCO3- при незначних концентраціях Ca2+. Мінералізація їх звичайно > 35 г/дм3.
Рідкіснолужні рудничні води з рН до 12 виявлено у гірничих виробітках масивів нефелінових сієнітів. Ці води мають CO3-Na, H3SO4-Na, H3SO4-F-Na склад і мінералізацію до 65 г/дм3.
Для багатьох геохімічних типів підземних вод характерними є часові зміни кислотно-лужних рівноваг і відповідно часові зміни рН.
Окислювально-відновлювальний потенціал (Eh) підземних вод – це показник ступеня окисленості або відновленості перемінно-валентних компонентів їхнього хімічного складу. Він слугує кількісною мірою здатності підземних вод до окислення і відновлення хімічних елементів. Величина окислювально-відновлювального потенціалу дозволяє судити про стан кожної окислювально-відновлювальної системи, що існує у підземних водах, а також визначає розподіл та міграційну здатність елементів з перемінною валентністю.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.