|
Виды внутренней энергии |
Методы анализа |
|||||
|
Объекты анализа |
||||||
|
Атомы, ионы |
Молекулы |
Агрегатированные системы |
Реакционные системы |
|||
|
Перенос (массы и заряда) |
Maсс - спектроскопия |
- |
- |
|||
|
Ядерная энергия: ядерный момент уровни нуклонов энергия связи ядра |
ЯМР - спектроскопия Спектроскопия Мессбауэра |
- |
- |
|||
|
Активационный анализ. |
- |
|||||
|
Энергия электронов: момент электрона уровни электронов Энергия ионизации |
ЭПР – спектроскопия Рентгеновская и электронная спектроскопия |
- - - |
- - - |
|||
|
Атомная спектроскопия |
Спектроскопия в видимой и УФ областях |
|||||
|
Энергия молекулы: Энергия вращения Колебательная энергия Энергия диссоциации |
- - - |
Микроволновая ИК - спектроскопия и комбинационное рассеяние |
- |
- |
||
|
Энергия решетки |
- |
- |
Термический анализ |
- |
||
|
Энергия реакции: химический потенциал электрохимический потенциал |
- - |
- - |
- - |
Химические методы анализа Электрохимические методы анализа |
||
Формулы
wQ = f(Q) = j(ΔE); (37)
ωc = F(c) G(I∆E) (38)
являются уравнениями связи между
измеряемыми величинами w,
соответствующими значениями энергии D Е (D Ekили DU) и I![]() , и аналитической информацией на основе какого-либо механизма
взаимодействия. Эти два уравнения составляют теоретическую основу
химического анализа. Именно в этих уравнениях со всей полнотой проявляется
отмеченная выше общность количественного и качественного анализов.
, и аналитической информацией на основе какого-либо механизма
взаимодействия. Эти два уравнения составляют теоретическую основу
химического анализа. Именно в этих уравнениях со всей полнотой проявляется
отмеченная выше общность количественного и качественного анализов.
Обозначим через Q величины, характеризующие природу компонентов и являющиеся при этом физическими свойствами конкретных компонентов, а через с — их концентрации. Именно такой смысл имеют Qи с в уравнениях (37), (38).
Конкретные значения физических величин (Q), используемых при проведении качественного анализа, а также концентрации компонентов (с) при проведении количественного анализа получают из уравнений связи этих величин в результате преобразования уравнений (37), (38):
Q = j (wQ ) (39)
с=Ф (w![]() ) (40)
) (40)
При проведении количественного анализа уравнения связи (40), как правило, не известны. Поэтому для их установления используют процедуру, названную градуировкой. Следует отличать градуировку, рассмотренную в разд. 4.5.1 как процедуру передачи размера единицы физической величины, от градуировки как способа нахождения уравнения связи между отличающимися физическими величинами. В последнем случае, используя вещества с известными значениями концентрации, экспериментально определяется зависимость (40).
Особое значение для метрологии имеют те редкие случаи, когда указанные уравнения связи известны в виде строгих математических уравнений, которые составляют теоретическую основу особой категории методов анализа — абсолютных методов анализа. В этом случае концентрация рассчитывается по измеренным значениям физических величин, входящих в конкретные уравнения связи. При этом отпадает необходимость в построении градуировочной характеристики.
Информацию о качественном
составе выражают константами веществ Q![]() .
При этом однородные константы можно расположить по их значениям от Q
.
При этом однородные константы можно расположить по их значениям от Q![]() до Q
до Q![]() .Такое последовательное
расположение классифицируют как одномерную аналитическую информацию
(рис. 134, а). Типичным примером такой информации служат длины волн, отдельных
элементов в спектре. В этом случае при проведении качественного анализа задачей
измерения является обнаружение в соответствующем интервале спектра искомых
конкретных длин волн. Результат качественного анализа представляется в форме
ответа "да—нет".
.Такое последовательное
расположение классифицируют как одномерную аналитическую информацию
(рис. 134, а). Типичным примером такой информации служат длины волн, отдельных
элементов в спектре. В этом случае при проведении качественного анализа задачей
измерения является обнаружение в соответствующем интервале спектра искомых
конкретных длин волн. Результат качественного анализа представляется в форме
ответа "да—нет".
Одномерная
аналитическая информация встречается и при проведении количественного анализа.
Например, при определении концентраций какого-либо компонента, который
характеризуется константой Q![]() ,
(рис. 134, б).
,
(рис. 134, б).
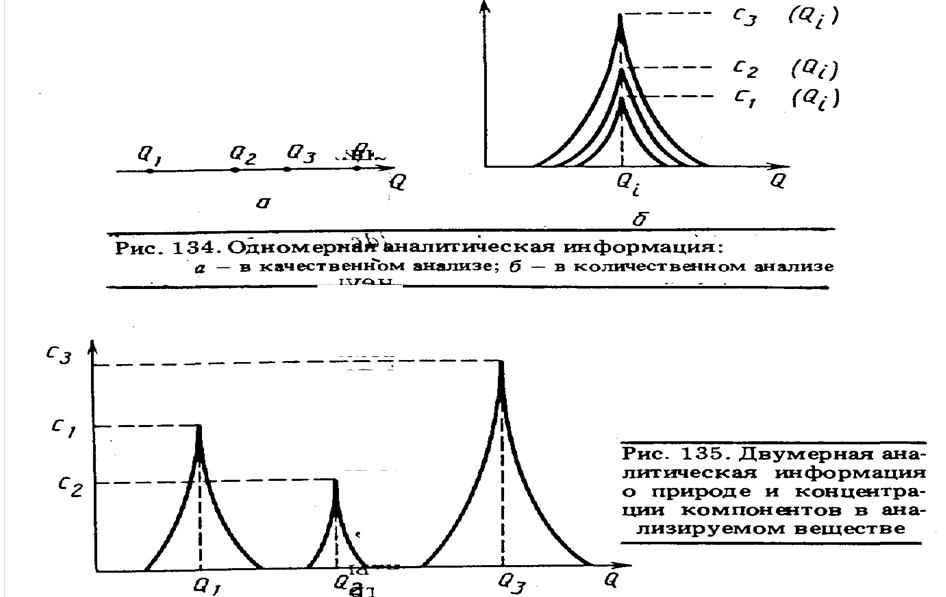
Если представить графически зависимость серии однородных
характеристических величин Q![]() ,
и соответствующих им интенсивностей w
,
и соответствующих им интенсивностей w![]() , являющихся согласно (40)
функцией концентрации, то взаимосвязь этих параметров дает регистрограмму
(спектрограмму, хроматограмму, полярограмму). Такие регистрограммы являются
двумерной аналитической информацией, содержащей одновременно
данные как о природе, так и о концентрации компонентов (рис. 135). Этот пример
служит еще одной иллюстрацией неразрывной связи количественного и качественного
анализа. Обнаружение сигналов при перемещении по оси Q
соответствует качественному анализу, а измерение w
, являющихся согласно (40)
функцией концентрации, то взаимосвязь этих параметров дает регистрограмму
(спектрограмму, хроматограмму, полярограмму). Такие регистрограммы являются
двумерной аналитической информацией, содержащей одновременно
данные как о природе, так и о концентрации компонентов (рис. 135). Этот пример
служит еще одной иллюстрацией неразрывной связи количественного и качественного
анализа. Обнаружение сигналов при перемещении по оси Q
соответствует качественному анализу, а измерение w![]() при фиксированных значениях Q
при фиксированных значениях Q![]() , дает данные о концентрации, т.
е. относится к количественному анализу.
, дает данные о концентрации, т.
е. относится к количественному анализу.
Для получения достоверных результатов метод химического анализа должен отвечать следующим требованиям.
1. Результаты измерений не должны быть искажены, т. е. измеряемая величина qa должна соответствовать характеристической константе компонента А. Это означает, что метод анализа должен быть избирательным (селективным) по отношению к этому компоненту. В таком случае мешающее влияние других компонентов, вызывающих появление систематической погрешности, может быть сведено к минимуму.
2. Средства измерений должны обеспечивать требуемую точность. При небольших концентрациях компонентов метод анализа в этом случае должен иметь высокую чувствительность, которая определяется следующим образом:
E=
F'(c) =dw![]() /dc.
/dc.
Все многообразие упругих и неупругих взаимодействий можно свести к нескольким основополагающим, как это представлено, например, на рис. 136, чтобы затем рассмотреть физические величины, охватываемые каждым из выделенных видов взаимодействий. Такой подход позволяет представить все многообразие аналитических методов в виде целостной системы.*
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.