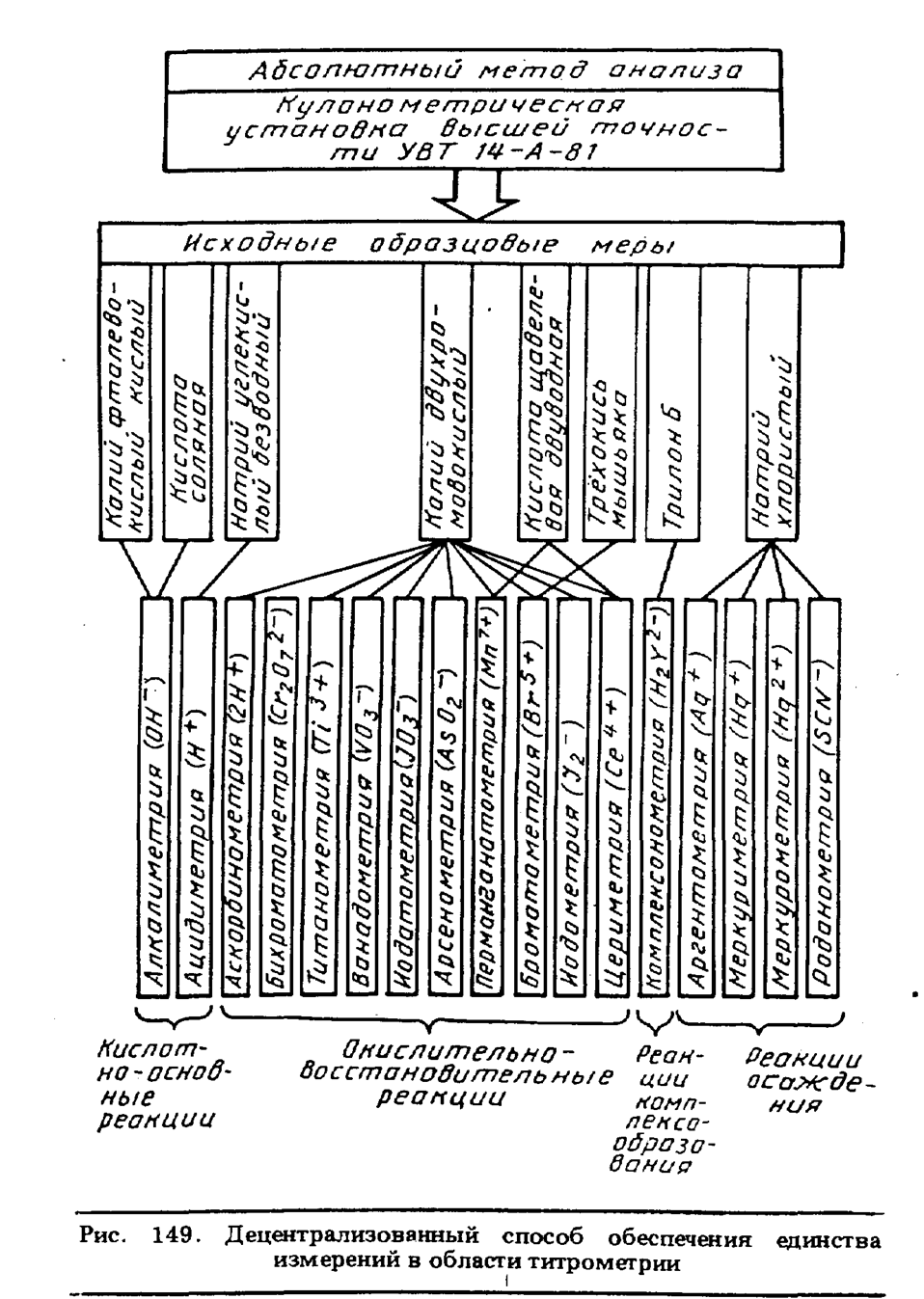
С помощью этих исходных образцовых мер единство измерений концентрации обеспечивается по схеме, приведенной на рис. 149.
Данные, представленные в табл. 38, заслуживают внимания и в том отношении, что они дают представление о требованиях к чистоте исходных образцовых мер концентрации. Однако здесь необходимо уточнить: степень чистоты зависит от индивидуальных особенностей веществ. Так, для большинства элементов она составляет 99,99 . . . 99,999 %, для солей неорганических веществ — 99,9 . . . 99,99 %. В то же время сложные органические соединения с содержанием 99 % также относятся к высокочистым.
Требования к чистоте исходных образцовых веществ определяются прежде всего метрологическими характеристиками средств измерений и перспективами развития приборостроения. В исходных высокочистых образцовых веществах, предназначенных для градуировки хроматографов, исходя из вышеизложенного требования, содержание основного компонента регламентируется на уровне не менее 99,95 %. Аналогичные требования предъявляются к исходным чистым газам, а также органическим и элементоорганическим соединениям для элементного анализа.
Второй подход к обеспечению единства измерений концентрации базируется на уже упоминавшемся постулате:
чистым веществам соответствует постоянство свойств. Как неоднократно отмечалось, вещество обладает бесконечным числом свойств. На этапе качественного анализа при формировании образа данного индивидуального вещества происходит отбор ряда свойств. В этом случае используется следствие из постулата, в соответствии с которым свойства чистых веществ являются их индивидуальными константами. Как правило, это — свойства, имеющие малую примесную чувствительность. Вместе с тем, есть ряд свойств, обладающих высокой примесной чувствительностью. По мере повышения степени чистоты вещества увеличивается перечень его свойств, в том числе и примесно чувствительных, значения которых не изменяются при дальнейшей очистке. Это позволяет утверждать, что такое вещество не содержит примесей выше известного предела. Следовательно, для веществ, прошедших глубокую очистку разными методами, можно принять их степень чистоты, равной 100 %.
Такой вывод основывается на обратном утверждении, вытекающем из указанного выше постулата, а именно: если чистым веществам соответствует постоянство свойств, то будет справедливо и утверждение, что постоянство свойств вещества свидетельствует об его чистоте.
Наиболее высокие требования к степени чистоты предъявляются только к весьма ограниченному числу веществ, представляющих основной компонент для приготовления образцовых мер в виде смесей с известной концентрацией других компонентов. Для этой категории веществ, если нет возможности определить их степень чистоты абсолютным методом анализа, целесообразно провести контроль на отсутствие тех компонентов, которые будут добавлены при приготовлении соответствующих образцовых мер.
Для веществ, используемых в качестве добавок, достаточна степень чистоты, не превышающая 99,99 %. Такая точность вполне может быть гарантирована для веществ, подвергнутых глубокой очистке различными методами, в результате которой ряд их примесночувствительных свойств достиг своего постоянства.
Сфера применения данного подхода по мере повышения требований к точности результатов измерения концентрации будет либо сужаться, либо потребуются дополнительные доказательства действительно глубокой очистки. В последнем случае это означает расширение числа примесночувствительных свойств, достигших своего постоянства.
Следует подчеркнуть, что второй подход при всех его недостатках с позиции метрологии позволяет обеспечить большую достоверность воспроизведения единиц концентрации, чем межлабораторная аттестация.
6.2.5. Образцовые меры концентрации и градуировка
Прежде чем перейти к метрологическим вопросам, связанным с передачей размера единиц концентрации от исходных образцовых mcj) к рабочим средствам измерений, необходимо обратить внимание на современные тенденции развития методов химического анализа. В наиболее общем виде они проявляются при наукометрических исследованиях, один из результатов которых представлен в табл. 39.
Таблица 39
|
Наименование метода |
Доля публикаций По годам , % |
|||
|
1965 |
1975 |
1979 |
1980 |
|
|
Хрома то графия |
24 |
27 |
30 |
36 |
|
Газовая хроматография |
8 |
9 |
11 |
13 |
|
Спектроскопия (ЭПР,ЯМР, фотометрия) |
36 |
36 |
37 |
40 |
|
Электрохимические методы |
10 |
20 |
13 |
12 |
|
Химические методы (гравиметрия, титрометрия и т. п.) |
30 |
17 |
20 |
12 |
• Основной вывод, вытекающий из табл. 39, — ускоренное развитие инструментальных методов и, соответственно, резкое возрастание числа аналитических приборов. В настоящее время доля химических методов стабилизировалась на уровне 3 %. Такое перемещение центра тяжести с химических методов анализа на инструментальные физические привело к обострению проблемы обеспечения единства измерений концентрации. Почему это произошло? Причина в том, что химические методы в своем большинстве относятся к абсолютным методам, а следовательно, проблемы образцовых мер концентрации для них практически не существует. В то же время практически для каждого физического метода, для каждого анализируемого этим методом компонента уравнение связи устанавливается в результате градуировки по образцовым мерам концентрации данного компонента. Особенностью физических методов является то, что точность результатов измерений не может быть выше точности градуировки.
Аналитические приборы в зависимости от подходов к их градуировке делятся на две группы: универсальные и анализаторы состава. Уравнения связи для приборов обеих этих групп не известны.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.