Циклоалканы (cyclo- CnH2n)
Основные продукты – молекулярный водород, циклоалкены, дициклоалканы. Регистрируются также продукты распада по С-С –связям и осколочные продукты.
 Для
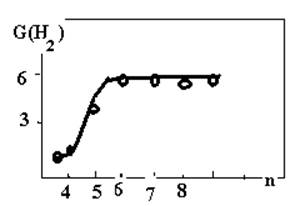
циклогексана – РХВ (Н2) – 5,5 мол-лы/100 эВ, циклогексена –
3,дициклогексила – 2, гексена – 0,4.
Для
циклогексана – РХВ (Н2) – 5,5 мол-лы/100 эВ, циклогексена –
3,дициклогексила – 2, гексена – 0,4.
Зависимость РХВ (Н2) от числа углеродных атомов в кольце.
Алкены и Циклоалкены
Радиолиз ненасыщенных органических соединений имеет следующие основные особенности:
1. РХВ (Н2) - существенно меньше, чем в алканах (не 5, а около 1), т.к. двойные связи – хороший акцептор атомов водорода. Следовательно работает только молекулярный, а не свободнорадикальный механизм образования водорода (акцептора атомарного водорода влияют мало).
2. Наличие двойной связи приводит к большим выходам димеризации (например, для гесена-2 димер образуется с РХВ = 5).
Полимеризация – это цепной процесс, который стадии зарождения, развития и обрыва цепи.
RH →R* R-CH=CH2 + R*→ R-CRH-C*H
R-CRH-C*H + R-CH=CH2→ R- (R-CRH-CH)CH-C*H и т.д.
Ароматические углеводороды
Они характеризуются высокой радиационной устойчивостью (G(Н2) = 0,02- 0,2 мол-л /100 эВ), что объясняется наличием сверхсопряженной электронной системы. Пи-электронная структура бензольных колец облегчает диссипацию энергии (её рассеивание). Поэтому возбуждение зачастую не приводит к химическим изменениям. Высокая стабильность бензольного кольца является причиной низких РХВ разрыва С-С –связей.
Атомы водорода, возникающие в реакции – С6Н6*→ С6Н5* +Н* быстро присоединяются к молекулам бензола, образуя циклогександиенильные СР –
С6Н6 + Н* → С6Н7*
Именно этой реакцией объясняется низкий РХВ молекулярного водорода.
РХВ димеров и других продуктов присоединения – порядка 1 мол-л /100 эВ.
При радиолизе конденсированных ароматических соединений (дифенил, трифенил и т.п.) выходы газообразных продуктов и димеров – еще меньше, чем для бензола. Именно поэтому полифенолы используются в качестве теплоносителей в некоторых видах ядерных реакторов.
Более того, ароматические соединения способны защищать от радиационного поражения другие молекулы «впитывая» возбуждение. Это так называемый эффект «губки».
Радиолиз углеводородов в присутствии кислорода
Основной особенностью этого процесса является образование перекисных и гидроперекисных радикалов:
Н* + О2 → НО2· НО2·+ НО2·→ НOOH + О2
R· + О2·→ RО2· RО2· + RH → ROOH + R· ( 25)
RО2· + R· → ROOR (26)
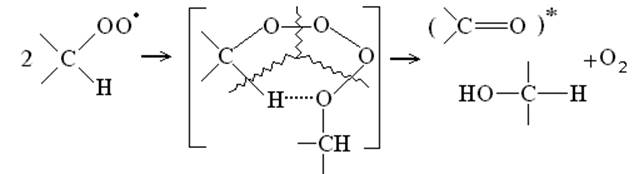
(27)
Т.о. новыми для нас молекулярными продуктами оказываются, прежде всего, перекисные соединения, причем трех видов - гидроперекиси (перекись водорода и ROOH) и органические перекисные соединения структуры ROOR .
Из курса «методы …» мы помним, что есть аналитический прием, позволяющий регистрировать эти соединения раздельно.
В качестве примера рассмотрим гексан и гептан.
РХВ суммы перекисных соединений составляет 2,6 молекул/100 эВ. При этом РХВ диалкилперекисей - 1 молекул/100 эВ , ROOH – 1,2 молекул/100 эВ перекиси водорода - 0,4 молекул/100 эВ.
Что касается реакции 25, то это, конечно цепной процесс, но в реальных системах развитие цепи наблюдается только при температурах существенно превышающих комнатную.
Как можно было заметить, продуктами реакции 27 являются альдегиды и спирты, которые также фиксируются в экспериментах.
Разбавленные водные растворы органических соединений
При радиолизе водных растворов органических веществ образуется, как правило, большой набор трудноидентифицируемых продуктов, что осложняет изучение механизмов протекающих при этом процессов. Поэтому мы остановимся только на относительно хорошо изученных сиситем.
Водные растворы алифатических спиртов
Спирты в водных растворах быстро реагируют с радикалами ОН* и О— (Константы скоростей реакций к порядка 108 – 109 л/моль.с. Гидратированные электроны взаимодействуют с ними гораздо медленнее. Основным каналом их превращения является реакция :
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.