Наряду с этим преимуществом дозиметр имеет недостатки:
- Погрешность – 15 % (при доверительной вероятности 0,95)
- “капризность”, которая определяется, прежде всего, низкой термической неустойчивостью ионов Cu+. Поэтому следует всегда пользоваться свежеприготовленными растворами.
Цериевый дозиметр
Цериевая дозиметрическая система представляет собой раствор соли Ce+4
В 0,4 М H2SO4, насыщенный воздухом. Под действием излучения Ce+4 восстанавливается до Ce+3. Использование этого метода дозиметрии предложено в 1952 г. В настоящее время установлено, что с помощью этой дозиметрической системы можно определять дозы до 106Гр ( 1 МГр).
При этом протекают следующие реакции:
Ce+4 + Н*→ Н+aq +Ce +3 G(Сe+3) = G (Н* ) +G (е-aq ) +2G(Н2О2 ) - G (ОН*)
Ce+4 + Н2О2→ Н+aq + Ce +3 + НО2* 2,3=0,6 + 3,05 +2 *0,8 - 2,95
Ce+4 + НО2*→ Н+aq + Ce +3 + О2
______________________________
Ce +3 + ОН*→ ОН-aq +Ce+4
В случае излучения Со-60 и других видов излучения с близкими величинами ЛПЭ G(Сe+3) = 2,3 – 2,5 ионов /100эВ. Он практически не зависит от энергии рентгеновского, гамма- и электронного излучения, по крайней мере в диапазоне от 0,25 до 24 МэВ (!).По данным последних измерений G(-Ce+3) = 2,30 ± 0,03 ионов/100 эВ.
Для излучений с большими ЛПЭ РХВ – несколько выше и мало зависит от вида заряженных частиц. Это делает использование цериевой дозиметрической системы перспективным для дозиметрии именно заряженных частиц.
При переходе от деаэрированной системы к насыщенной воздухом РХВ увеличивается на 2,1%, а к насыщенной кислородом – на 5,1%.
Малая зависимость РХВ от концентраций Ce+4 и Ce +3 делает этот дозиметр пригодным для измерения больших поглощенных доз.
 Однако
существенным недостатком данной дозиметрической системы является её высокая
чувствительность к примесям. Органические вещества даже в малых количествах
приводят к значительному увеличению РХВ. Сильно влияют также и некоторые
неорганические вещества – Tl+, NO3-,
Br – и др. Поэтому при приготовлении цериевого дозиметра
необходимо применять трижды перегнанную воду, дополнительно очищенную
радиолизом.
Однако
существенным недостатком данной дозиметрической системы является её высокая
чувствительность к примесям. Органические вещества даже в малых количествах
приводят к значительному увеличению РХВ. Сильно влияют также и некоторые
неорганические вещества – Tl+, NO3-,
Br – и др. Поэтому при приготовлении цериевого дозиметра
необходимо применять трижды перегнанную воду, дополнительно очищенную
радиолизом.
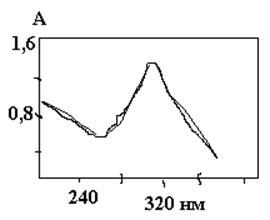
Наибольшее распространение получил спектрофотометрический метод регистрации, когда количество образовавшегося Ce +3 определяют по убыли Ce+4. Максимум полосы поглощения Ce+4 расположен при 320 нм. При этой длине волны молярный коэффициент экстинкци, по данным разных авторов составляет от 5550 до 6100 л/моль.см.
Оптическая плотность раствора с концентрацией Ce +3 2.10-4М в 0,4 М серной кислоте составляет А = 1,12. Очевидно, что при использовании более концентрированных растворов (для измерения больших поглощенных доз) растворы перед измерением следует разбавлять серной кислотой.
Если применять спектрофотометрический метод регистрации, то в стандартных условиях можно зарегистрировать 100 Гр. Флуоресцентный метод анализа Ce +3 позволяет снизить порог чувствительности до 0,5 Гр.
Верхний предел измерений дозы зависит от начальной концентрации
Ce +4 .и может достигать 1 Мгр.
(дополнительно можно прочитать о глюкозном дозиметре- угол вращения плоскости поляризации, о щавелевокислотном – разложение, о бихроматном – убыль бихромат иона с образованием Cr +3,хлорбензольном …)
¨ во-первых, многие органические вещества используются в качестве экстрагентов и разбавителей при переработке ядерного топлива и, следовательно подвергаются радиолизу, механизм которого необходимо знать;
¨ во-вторых, некоторые ароматические соединения, вследствие своей высокой радиационной стойкости, являются перспективными теплоносителями в ядерных реакторах (мал РХВ разрушения);
¨ в-третьих, знание РХ превращений органических веществ важно для разработки новых экономичных методов РХ синтеза различных соединений;
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.