Проводя дозиметрию ИИИ, следует придерживаться следующих правил:
1. Материал ячейки должен быть химически инертен по отношению к дозиметрической системе (ни катализа, ни ингибирования).
2. При фотонном излучении толщина стенок должна быть меньше пробега вторичных электронов, генерируемых в стенке ячейки (например, для Со60 для стекла d<1,5 мм, для ПЭ - d<3 мм,), иначе – завышенный результат за счет регистрации вторичных электронов из стенки ячейки.
3. Для жидких дозиметрических систем размеры ячейки должны быть значительно больше пробегов вторичных электронов в жидкости, т.е. должно соблюдаться электронное равновесие (реальный вклад – 1-6 %).
4. В случае дозиметрии потоков заряженных частиц, толщина стенки д.б. много меньше пробега частицы в ней, т.е. необходимо минимизировать поглощение ИИ в стенке. При этом не только для корпускулярного, но и для фотонного излучения необходимо учитывать ослабление его потока в самой дозиметрической среде.
Кроме того, необходимо, чтобы дозиметрическая и исследуемая системы были в одинаковом агрегатном состоянии (недопустимо газ – жидкость).
В общем виде величину поглощенной дозы определяют по формуле:
D= 9,65 . 10 6 ΔС/G ρ ( Гр)
Для фотонного излучения остается учесть только различия в характеристиках поглощения энергии ИИ:
Dиссл = Dдозим (μпогл/ρиссл) / (μпогл/ ρдоз) = Dдозим (Z/A)иссл / (Z/A)дозим
Где - (μпогл/ρиссл) – массовые коэффициенты поглощения энергии, а
(Z/A) – эффективные атомные номера исследуемой и дозиметрической систем.
Химические дозиметры на основе водных растворов
Для разбавленных водных растворов характерно косвенное действие ИИ, т.е. радиолиз не самих молекул и ионов растворенного вещества, а действие на них продуктов радиолиза воды.
Проявляется это в виде окислительно-восстановительных реакций, газовыделения, изменения рН системы, образования осадков и т.д.
Дозиметр Фрикке
Это система, содержащая (0,4 М Н2SО4 + О2 + (NH)2SO4 . FeSO4 .6H2O – соль Мора + NaCl 0,06 г/л)
Для гамма-излучения Со60 и других близких по энергии излучений, РХВ, определенный калориметрическим, ионизационным, и другими абсолютными методами составляет 15,4 – 15,6 молекул на 100 эВ
Поскольку в системе есть протоны и кислород, протекают реакции:
е-aq+ Н+→ Н* (1) О2 + Н*→ НО2* (2)
Далее :
Fe 2+ + ОН*→ Fe3+ + ОН- (3)
Fe 2+ + НО2*→ Fe3+ + Н2О2 (4)
Fe 2+ + Н2О2 + Н+aq → Fe3+ + ОН-aq + ОН* (5)
Поскольку ОН* - 1, Н2О2 - 2, а е-aq и Н* - 3 ( за счет реакции 4), то
G(Fe+3) = G (ОН*) +2G(Н2О2 ) + 3 (G (Н* ) +G (е-aq ) ) =
2,95 + 2 . 0,8 + 3 (3,05 + 0,6) = 15,5 ионов/ 100 эВ
Добавка NaCl в концентрации 10-3 М необходима для подавления влияния органических примесей, поскольку образующиеся радикалы Cl значительно быстрее реагируют с ионами двухвалентного железа, чем с органическими веществами.
Cl- + ОН*→+ Cl*+ ОН- Cl*+ Fe 2+ → Fe3+ +Сl-
Регистрацию ионов трехвалентного железа проводят спектрофотометрически при 304 нм (ε = 2205 л/ моль. см).
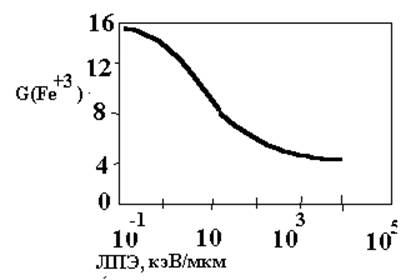 Влияние ЛПЭ
Влияние ЛПЭ
РХВ практически не зависит от ЛПЭ для рентгеновского, гамма и быстрых электронов в диапазоне от 0,66 до 30 МэВ, поскольку в этих случаях ЛПЭ меняется слабо.
Но при работе с другими видами излучения это не так.
(рис. 7.4. стр. 294 Пик)
Влияние мощности дозы
РХВ не зависит от мощности дозы до 10-6 Гр/с (что сопоставимо со скоростью самопроизвольного окисления ионов кислородом при комнатной температуре).
Выше 106 Гр/с наблюдается уменьшение РХВ, но поскольку при непрерывно облучении при больших мощностях дозы проявляется влияние и других факторов, то желательно работать с этой системой при мощностях дозы не более 10 Гр/с.
Влияние концентраций реагентов
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.