Важную структурную роль ион цинка играет в белок-нуклеиновом и белок-белковом взаимодействиях, осуществляемых так называемыми «цинковыми пальцами». Такое название получила супервторичная структура белка, образованная приблизительно из тридцати аминокислотных остатков и ионов цинка (одного или нескольких), тетраэдрически координированных остатками гистидина, цистеина и изредка аспартата. В настоящее время известно более десятка классов структур «цинковых пальцев». Они играют различную роль в функционировании клетки, но они все принимают участие во взаимодействии белка с нуклеиновыми кислотами (ДНК и РНК), липидами, другими белками. Часто белки содержат несколько структур «цинковых пальцев», относящихся к тому же к разным классам. Наиболее изучены «цинковые пальцы» в составе факторов транскрипции.
Классический «цинковый палец» имеет структуру С2Н2, где ион цинка координирован двумя остатками цистеина и двумя гистидина, и взаимодействует с 2−4 парами гетероциклических оснований в структуре нуклеиновой кислоты (схема 55).
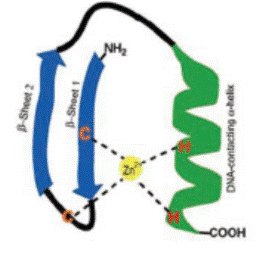
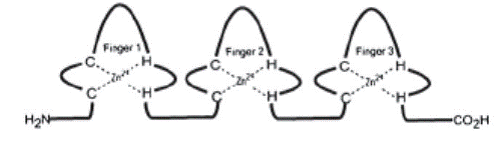 (55)
(55)
На схеме 56 приведены некоторые структуры «цинковых пальцев», встречающихся в составе различных белков.
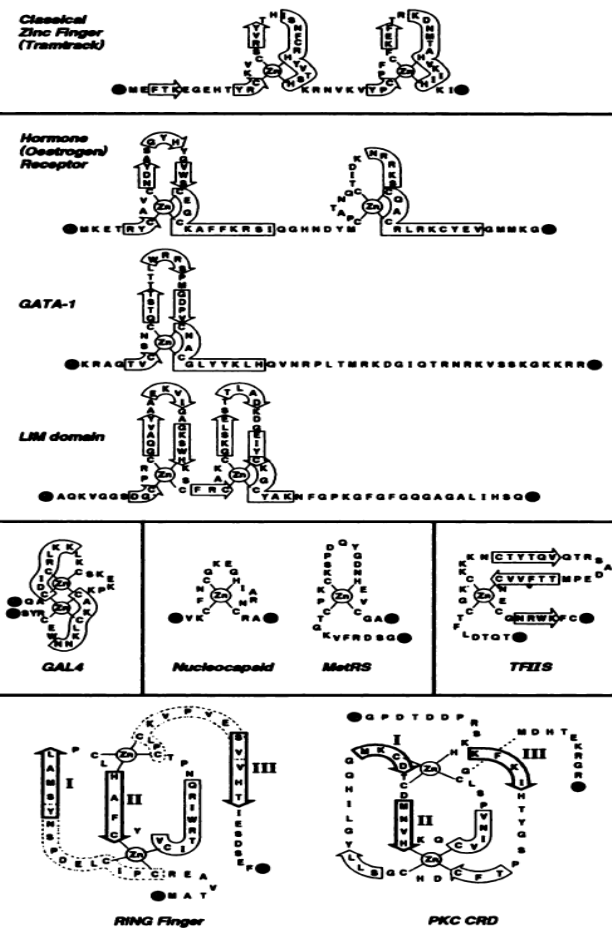 (56)
(56)
Структурную роль ионы цинка играют и в инсулине: они необходимы для образования кристаллических форм (гексамеров) инсулина, в виде которых этот гормон депонируется β-клетками поджелудочной железы (схема 57).
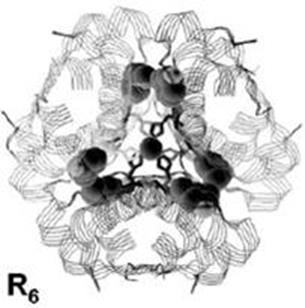 (57)
(57)
Цинк также необходим для обоняния и нормального восприятия вкуса продуктов. Он входит в состав белка густина (от английского слова "gust", что значит "острый приятный вкус"), вырабатываемого околоушной слюнной железой и играющего важную роль в процессах вкусовой чувствительности. Густин, идентифицированный как карбоангидраза VI, специфически связывается с мембранами вкусовых сосочков и регулирует поступление в них питательных веществ.
Цинк оказывает влияние на усвоение организмом витамина А. В отсутствие достаточного количества этого металла организм не может синтезировать белок, транспортирующий витамин А через стенку кишечника и освобождающий его в кровь. Это приводит к уменьшению поступления витамина А к тканям. А дефицит витамина А препятствует усвоению цинка.
Поскольку цинк тормозит высвобождение из клеточных мембран гидролитических ферментов (катепсина D, коллагеназы), контролирующих распад поврежденных тканей, он способствует заживлению ран. Активируя ферменты нуклеинового и белкового синтеза, цинк в случае дефицита вызывает задержку деления клеток и роста организма. Но это свойство цинка может обернуться и злом для организма, так как злокачественные клетки для своего роста требуют большого количества данного металла. В случае дефицита цинка наблюдаются также выпадение волос, ухудшение памяти, снижение внимания, угнетение процессов сперматогенеза и торможение развития первичных и вторичных половых признаков, токсикозы беременности. Ион цинка обладает высоким сродством к сульфгидрильным группам, которые, как известно, определяют третичную структуру и функции белка. Цинк защищает эти группы от окисления ионами железа и меди, тем самым стабилизируя пространственную структуру белка и постоянство проявления его функций.
Таким образом влияние иона цинка на метаболизм организма огромно и затрагивает разнообразные функции.
6.1.9. Галоиды. Соединения галоидов: хлора, фтора, брома и йода, широко представлены в различных живых организмах и выполняют разнообразные функции. Хлор относится к группе макроэлементов, остальные галоиды являются микроэлементами.
6.1.9.1. Хлор. Наиважнейшая функция хлора в организме заключается в образовании соляной кислоты, играющей большую роль в процессе пищеварения. Подробно этот процесс был рассмотрен нами в п. 5.1.1. «Части 5. Биохимия процессов пищеварения». Соляная кислота секретируется в просвет желудка обкладочными клетками, при этом ион хлора поступает из крови в обмен на ион бикарбоната, синтезируемого под действием карбоангидразы согласно уравнению (схема 58):
CO2 + H2O « H2CO3 « H+ + HCO-3 (58)
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.