
Таким образом, карбоксильная группа в молекулах карбоновых кислот проявляет отрицательный индукционный эффект (-I-эффект).
1.6.Химические свойства
Свойства карбоновых кислот обусловлены в первую очередь присутствием в их молекулах карбоксильной группы.
1.6.1.Кислотные свойства
Карбоновые кислоты в водных растворах диссоциируют:
![]() R-COOH + H2O
R-COO- + H3O+
R-COOH + H2O
R-COO- + H3O+
![]()
Однако по сравнению с минеральными кислотами, такими как HCl, HBr, HI, H2SO4, HNO3, H3PO4 и др., органические кислоты намного слабее, но более сильные, чем угольная кислота. Поэтому минеральные кислоты вытесняют карбоновые кислоты из их солей, а карбоновые кислоты в свою очередь вытесняют угольную кислоту из ее солей. Согласно теории кислот и оснований Бренстеда-Лоури, такие соединения, как вода, спирты, ацетилен, аммиак, амины, углеводороды, можно рассматривать также как кислоты. Однако они по сравнению с карбоновыми кислотами намного слабее. Относительная кислотность этих соединений изменяется в таком порядке:
HCl > R-COOH > H-OH > R-OH > HCºCH > NH3 > R-H
Так, кислотные свойства атома водорода гидроксильной группы карбоксила карбоновой кислоты за счет (-)I-эффекта и эффекта p,p-сопряжения -CO- группы значительно сильнее, чем водорода гидроксила молекулы воды. Вместе с тем, кислотные свойства водорода группы OH спирта, благодаря (+)I-эффекта алкильной группы проявляются слабее, чем у гидроксила воды. Сказанное подтверждается значением КД25 для этих веществ:

Кислотные свойства карбоновых кислот (R-COOH) зависят от природы и строения алкильного радикала (-R), присутствия заместителей в его углеродной цепи. Группы R- с положительным электронным эффектом уменьшают величину частичного заряда d+ на карбонильном C-атоме и тем самым уменьшает его электроноакцепторное действие на группу –OH. Это приводит к уменьшению силы карбоновой кислоты. Поэтому в гомологическом ряду монокарбоновых кислот муравьиная кислота, в молекуле которой рядом с карбоксильной группой нет углеводородного радикала с положительным электронным эффектом, является наиболее сильной. Уксусная кислота в сравнении с муравьиной в десять раз слабее, поскольку в ее молекуле есть метильный радикал, который проявляет (+)I-эффект. Атомы и группы атомов с отрицательным электронным эффектом увеличивают величину заряда d+ на карбонильном C-атоме и тем самым усиливают электроноакцепторное действие карбонила на группу –OH. Это обусловливает значительное повышение силы карбоновой кислоты. Поэтому хлоруксусная кислота приблизительно в 20 раз сильнее, чем уксусная. Таким образом, группы R- с положительным электронным эффектом уменьшают, а с отрицательным электронным эффектом увеличивают силу карбоновых кислот. Это убедительно подтверждает сравнение значений рКк карбоновых кислот, которые содержат R- разной электронной природы (стрелками показано смещение электронов в молекуле кислоты):
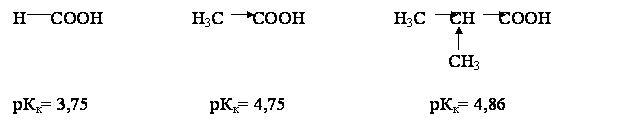 |
|
 |
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.