Mg + HCl = MgCl2 + H2
10. Взаємодія металів з солями:
Fe + CuSO4 = FeSO4 + Cu
Хімічні властивості солей.
1. Метали, які мають менше алгебраїчне значення стандартного електродного потенціалу, витісняють із солі метал, який має більше алгебраїчне значення стандартного електродного потенціалу:
Zn + FeSO4 = Fe + ZnSO4.
2. Солі взаємодіють з кислотами:
CuSO4 + H2S = CuS¯ + H2SO4
3. Солі взаємодіють з лугами:
CuSO4 + 2KOH = Cu(OH)2¯ + K2SO4
4. Солі взаємодіють між собою:
CaCl2+Na2СO3=CaCO3¯+ 2NaCl
Три останні типи взаємодій відбуваються у випадку, коли утворюються гази (SO2, CO2) або нерозчинні речовини ( Cu(OH)2, CaCO3).
Приклад 1. Визначить масову долю фосфору в простому і подвійному суперфосфаті.
Розв’язок:
1. М Са3(РО4)2 ? М Са (Н2РО4)2 - ?
М Са3(РО4)2 = 40,1.3 + 31.2 + 16.8 = 120,3 + 62 + 128 = 310,3 (г/моль)
М Са (Н2РО4)2 = 40,1 + 1.4 + 31.2 + 16.8 = 234,1 (г/моль)
2. w (Р) у Са3(РО4)2 - ? w (Р) у Са (Н2РО4)2 - ?
w (Р) = 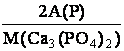 =
=![]()
![]() = 0,20 ( 20,0 %)
= 0,20 ( 20,0 %)
w (Р) = 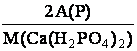 =
= ![]() =
0,265 ( 26,5 %)
=
0,265 ( 26,5 %)
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.