Результаты этого долговременного клинического исследования демонстрируют, что включение в терапию b2-агониста длительного действия, формотерола, стойко уменьшают обструкцию дыхательных путей и ночные симптомы и сокращают потребность в дополнительном применении препаратов для облегчения симптомов у детей, у которых все еще сохраняется симптоматика, несмотря на терапию противовоспалительными препаратами. Эти данные также подтверждают, что регулярное применение мощного бронходилататора длительного действия является безопасным и хорошо переносится при условии, что пациенты также получают ингаляционные кортикостероиды в качестве противовоспалительной терапии. Несмотря на возможные причины наблюдавшегося в ходе исследования более высокого числа СНЯ в группе формотерола, которые мы обсуждали, имеются основания для дальнейших исследований по изучению возможности маскирования формотеролом воспаления дыхательных путей. И пациенты, и врачи должны понимать, что ни объем противовоспалительной терапии, ни регулярность мониторирования течения заболевания не должны снижаться, даже если достигнуто улучшение симптомов и функции легких на фоне назначения b2-агонистов длительного действия.
БЛАГОДАРНОСТИ
Авторы выражают благодарность другим членам Международной исследовательской группы по оценке Форадила при бронхиальной астме в педиатрии (International Study Group on Foradil Evaluation in Pediatric Asthma), поименованным ниже (по странам): Аргентина: J.A. Avila, А.М.С. Balanzat, G.J. Bustos, С. Caceres.J.C.F. Casas, H. Diaz Velez, B.L.O. Gil, W.H. Linares; Чили: I.S. Diaz, R. Sepulveda Moncayo; Испания: N.C. Barroso, C.V. Cotdero, M.N. Merino, EG. Perez-Yarza; Соединенные Штаты: Е.А. Bronsky, P. Chervinsky, D.M. Cypcar, T.B. Edwards, S.M. Fries, S.P. Galant, J. Grossman, W.V. Kinnard, S.M. Kreitzer, B. Lanier, M. Lawrence, A. Malanga, H. Milgrom, A.S. Nayak, N.K. Ostrom, D.S. Pearlman, S.J. Pollard, B.M. Prenner, M.E. Ruff, N. Segall, D.L. Southern, B. Stone, H.H. Windom.J.D. Wolfe, J.A. Yarborough.
Таблица 3.
Оценка различий терапевтических групп с указанием соответствующих 95% доверительных интервалов и величин Р для средних утренних и вечерних значений ПСВ до принятия препарата за все доступные дни первых 3 месяцев и всего 12-месячного периода лечения.
|
Различия терапевтических групп |
Оценка (л/мин)* |
95% Доверительный интервал (л/мин) |
Величина Р |
|
Месяцы 1-3 (N - 513) Средняя утренняя ПСВ до приема препарата Ф24-ПЛ |
21 |
15-27 |
< 0,0001 |
|
Ф12-ПЛ |
16 |
10-22 |
< 0,0001 |
|
Ф24-Ф12 |
5 |
-2-11 |
0,1406 |
|
Средняя вечерняя ПСВ до приема препарата Ф24-ПЛ |
19 |
13-25 |
< 0,0001 |
|
Ф12-ПЛ |
14 |
8-20 |
< 0,0001 |
|
Ф24-Ф12 |
5 |
-1-11 |
0,0917 |
|
Месяцы 1-12 (N = 513) Средняя утренняя ПСВ до приема препарата Ф24-ПЛ |
19 |
12-26 |
< 0,0001 |
|
Ф12-ПЛ |
12 |
5-19 |
0,0009 |
|
Ф24-Ф12 |
8 |
1-15 |
0,0281 |
|
Средняя вечерняя ПСВ до приема препарата Ф24-ПЛ |
16 |
10-23 |
< 0,0001 |
|
Ф12-ПЛ |
8 |
2-15 |
0,0152 |
|
Ф24-Ф12 |
8 |
1-15 |
0,0205 |
|
* По модели ANCOVA: средняя ПСВ=вид терапии + страна + центр (страна) + пол + исходное значение (средняя ПСВ за последние 7 дней вводного периода). Ф24, формотерол 24 мкг; Ф12, формотерол 12 мкг; ПЛ, плацебо. |
|||
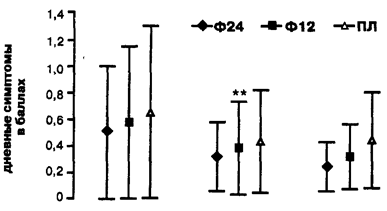
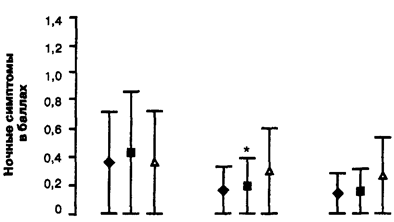
Балльная оценка симптомов в зависимости от терапии
![]()
Иллюстрация 3.
Балльная оценка дневных (вверху) и ночных (внизу) симптомов бронхиальной астмы для каждой терапевтической группы. Данные представлены как медианы и средний межквартильный разброс значений за последние 7 дней вводного периода, за первые 3 месяца терапии (месяцы 1-3) и за весь период лечения (месяцы 1-12). Ф24- формотерол 24 мкг; Ф12 - формотерол 12 мкг, ПЛ - плацебо. *.Р - 0.041 по сравнению с плацебо: **.Р - 0.030 по сравнению с плацебо.
Таблица 4. Серьезные и несерьезные нежелательные явления и преждевременное прекращение исследования
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.