где C - электрохимический эквивалент, г/А·ч; I - ток, А; t - время осаждения, ч; М и Z - молярная масса (г/моль-ион) и валентность осаждаемого элемента; F - постоянная Фарадея, определяемая произведением количества элементарных частиц в одном моле вещества (постоянная Авогадро 6,022·1023 моль-ион-1) на значение элементарного заряда 1,602·10-19 Кл, отсюда F = 6,022·1023·1,602·10-19=96484 Кл/моль.
На катоде кроме осаждения металла протекают сопутствующие процессы: выделение водорода, восстановление металла до более низкой валентности, восстановление органических веществ, попавших в электролит. Поэтому действительная масса металла, выделившегося на катоде, будет меньше его массы, рассчитанной по формуле (2.7). Отношение массы действительно выделившегося металла на электроде к теоретически возможному его количеству называется коэффициентом выхода по току a, значение которого всегда меньше единицы.
Толщину электролитического осадка h определяют по формуле:
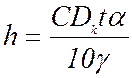 ,
мм, (2.24)
,
мм, (2.24)
где Dk = I/Sk - плотность тока, А/дм2; Sk - площадь катода, дм2; g - плотность осаждаемого металла, г/см3.
Время осаждения электролитического осадка определяют по формуле:
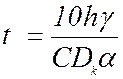 ,
ч. (2.25)
,
ч. (2.25)
Область применения и оценка. Электрохимические покрытия применяют в ремонтном производстве при восстановлении деталей с небольшими износами, но с высокими требованиями к износостойкости, твердости и сплошности покрытия и прочности его соединения с основой. Считают, что около 65 % деталей ремонтного фонда имеют износ на сторону до 0,14 мм.
По сравнению с другими процессами нанесения покрытий электролиз обеспечивает: сохранение структуры материала детали за счет отсутствия вложения тепла в него; высокую износостойкость и твердость покрытий; равномерную их толщину; возможность получения покрытий с заданными, изменяющимися определенным образом по их толщине физико-механическими свойствами; большое количество одновременно восстанавливаемых деталей и возможность автоматизации; использование недефицитных материалов. Однако, скорость нанесения покрытий низкая, процесс многооперационный и сопровождается большим расходом энергии и воды и загрязнением сточных вод ионами тяжелых металлов.
Виды электролиза В зависимости от видов материалов наносимых покрытий электрохимические процессы делятся на железнение, хромирование, цинкование, кадмирование, никелирование и др. В ремонтном производстве наибольшее распространение получили первые три процесса. В свою очередь, первые два процесса обеспечивают получение износостойких покрытий, а цинкование – как износостойких, так и защитных покрытий. Цинк обеспечивает надежную катодную защиту стальных изделий.
Железнение. Применяют при восстановлении поверхностей деталей, изношенных более чем на 0,2 мм и требующих высокой поверхностной твердости. Восстанавливают трущиеся шейки и шейки под неподвижные посадки, поверхности отверстий под втулки и обоймы подшипников в стаканах и корпусных деталях и другие элементы.
Наиболее распространен электролит железнения из хлористого железа (300...500 г/л) и соляной кислоты (2...3 г/л) в воде. Присутствие свободной HCl предупреждает образование гидрооксидов, которые загрязняют электролит и снижают качество покрытия
Для поддержания необходимой массовой доли ионов железа применяют растворимые аноды из армко-железа, площадь которых меньше площади катодов примерно в два раза.
Во время электролиза на электродах протекают следующие процессы: восстановление на катоде - разряд ионов железа Fe2+ + 2e = Fe, выделение водорода 2H+ + 2e = H2, восстановление трехвалентного железа Fe3+ + e = Fe2+; окисление на аноде - растворение железа Fe - 2e= Fe2+, окисление двухвалентного железа Fe2+ - e = Fe3+, выделение кислорода.
Катодная плотность тока при железнении составляет 5...15 А/дм2, а выход по току - 85…95 %.
Электролитическое железо по своему составу приближается к малоуглеродистой стали с содержанием углерода 0,03…0,06 %, однако его кристаллическая решетка напряжена, а по своим физико-механическим свойствам осадки близки к закаленной стали.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.