|
Образец исследуемого пива |
Дата проведения опыта |
рН |
Еh |
Длина волны, λ |
T,оС |
Оптическая плотность,D |
|
«Ханс» светлое |
11.12.2007 |
4,58 |
148,6 |
420 |
20,0 |
0,497 |
|
«Балтика»светлое |
11.12.2007 |
4,24 |
167,4 |
420 |
21,0 |
0,311 |
|
«Ханс» светлое |
12.12.2007 |
4,57 |
146,5 |
420 |
20,2 |
0,481 |
|
«Балтика»светлое |
12.12.2007 |
4,27 |
165,2 |
420 |
19,2 |
0,319 |
|
«Ханс» светлое |
13.12.2007 |
4,55 |
149,3 |
420 |
19,3 |
0,481 |
|
«Балтика»светлое |
13.12.2007 |
4,26 |
165,6 |
420 |
19,0 |
0,313 |
2.4 Определение окислительно-восстановительной способности пива
Материалы и оборудование:
рН-метр лабораторный «HANNA pH 213», спектрофотометр лабораторный «ЮНИКО – 1201».
Сущность метода заключается в измерении оптической плотности раствора по истечению 60 с после прибавления 2,6-дихлорфенолиндофенола. Редуктоны восстанавливают его красные кислые или голубые щелочные растворы в бесцветные лейкосоединения:

2,6 - дихлорфенолиндофенол 2,6 -дихлорфенолиндофенол
(натриевая соль) (лейкоформа)
Реактив имеет синюю окраску при рН 6,которая при рН 5,5 переходит в красную.
2.4.1. Приготовление реактивов
2.4.1.1 Нормализация раствора 2,6- дихлорфенолиндофенол (С12НСl2NО2Nа)
Материалы и оборудование
Серная кислота, Н2SО4, 2 % раствор
Калий йодистый, КI, х.ч.
Крахмал, 1 % раствор
Йодноватокислый калий, КIО3, 0,001 н раствор
Микробюретка,V= 1,00 мл
Цилиндр, V=50 мл
Пипетка Мора, V=5 мл
Ацетатный буферный раствор, рН = 4,4
В 50 мл 2 %-го раствора серной кислоты вносили несколько кристаллов аскорбиновой кислоты (1 – 1,5 мг). 5 мл полученного раствора титровали из микробюретки исследуемым раствором 2,6 - дихлорфенол – индофенола до появления розового окрашивания.
Параллельно 5 мл раствора аскорбиновой кислоты, с добавлением нескольких кристаллов йодистого калия (КI), оттитровывали 0,001 н раствором иодноватокислого калия (КIО3) в присутствии крахмала до появления голубой окраски.
Титр раствора 2,6 - дихлорфенол–индофенола Х вычисляли по формуле:
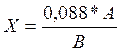
где А – количество миллилитров 0,001 н раствора иодноватокислого калия, израсходованное на титрование раствора аскорбиновой кислоты;
В - количество миллилитров раствора 2,6-дихлорфенолиндофенола, пошедшего на титрование, мл
0,088 – масса аскорбиновой кислоты, эквивалентная 1 мл 0,001н раствора КIО3, мг.
(0,088 * 0,019) / 0,135 = 0,0123 г/мл (титр)
12,385 г/л – концентрация готового раствора 2,6 - дихлорфенол – индофенола.
Пиво перед анализом выдерживали при температуре 20 оС. В пробирку вносили 10 мл дегазированного пива и с помощью микропипетки осторожно по краю пробирки приливали 0,25 мл 12,385М раствора 2,6-дихлорфенол- индофенола. Содержимое дважды энергично встряхивали и точно через 60 с определяли оптическую плотность раствора при длине волны 520 нм. l = 10 мм.
Параллельно проводили холостой опыт, внося в пробирку вместо пива 10 мл фосфатного буферного раствора. При исследовании пива рН буферного раствора составляло 4,35 – 4,40.
Окислительно – восстановительную способность определяли по формуле:
![]()
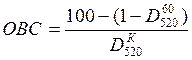
где ![]() -
оптическая плотность образца пива.
-
оптическая плотность образца пива.
![]() - оптическая плотность холостого раствора
при соответствующем рН
- оптическая плотность холостого раствора
при соответствующем рН
(Мальцев, 1976).
3. РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Большое влияние на стабильность готового пива оказывают физико-химические характеристики напитка и соответственно они влияют на химический состав напитка.
Основным фактором, влияющим на стойкость напитка брожения, является наличие кислорода, который, попадая в напиток даже в небольших количествах, активно взаимодействует с компонентами сусла и пива, а так же инициирует свободно-радикальные процессы. В результате – накопление продуктов соответствующих реакций, то есть наблюдается порча напитка. вещества способны либо нейтрализовать действие кислорода, либо подвергаться окислению настолько быстро (с очень высокой скоростью), что кислород не успевает вступить в реакцию с другими компонентами раствора.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.