![]() ;
;
![]() ;
;
![]() ;
;
![]() ;
;
![]()
![]() .
.
Скорость реакции восстановления оксидов гидразином существенно возрастает с повышением температуры среды и зависит от рН. Полностью обескислородить конденсат вводом в него гидразина невозможно, так как при низких температурах реакция между кислородом и гидразином практически не протекает и в воде сохраняется кислород и избыток гидразина, а при этом коррозия латуни усугубляется. Избыточный гидразин в условиях работы котла разлагается с образованием аммиака и азота:
![]() ;
;
![]() .
.
![]() Разложение гидразина практически
завершается в котловой воде, где содержание его аналитически не обнаруживается.
Разложение гидразина практически
завершается в котловой воде, где содержание его аналитически не обнаруживается.
Начальная дозировка N2H4 до появления избытка гидразина в воде равна:
![]() , мкг/кг, (8-1)
, мкг/кг, (8-1)
где ![]() ,
,![]() ,
,![]() ,
,![]() - нормативное содержание в питательной
воде соответственно кислорода, железа ,меди, нитритов и нитратов мкг/кг
(таблица П.2 Приложения). Нормальная дозировка гидразина в 1,5-2 раза меньше
начальной и должна обеспечить избыток гидразина
- нормативное содержание в питательной
воде соответственно кислорода, железа ,меди, нитритов и нитратов мкг/кг
(таблица П.2 Приложения). Нормальная дозировка гидразина в 1,5-2 раза меньше
начальной и должна обеспечить избыток гидразина![]() перед
экономайзером (в соответствии с ПТЭ) 20 - 60 мкг/кг.
перед
экономайзером (в соответствии с ПТЭ) 20 - 60 мкг/кг.
Количество гидразина в питательной воде с учётом потерь в КПТ:
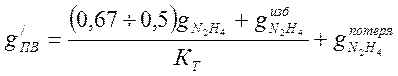 ,
мкг/кг, (8-2)
,
мкг/кг, (8-2)
где ![]() - температурный коэффициент разложения ,
для барабанных котлов выского давления (14 МПа) равен 0,8 ;
- температурный коэффициент разложения ,
для барабанных котлов выского давления (14 МПа) равен 0,8 ; ![]() - потеря гидразина в деаэраторе (из опыта
эксплуатации » 17мкг/кг).
- потеря гидразина в деаэраторе (из опыта
эксплуатации » 17мкг/кг).
Общий расход гидразина определяется :
![]() , г/ч , (8-3)
, г/ч , (8-3)
где ![]() , т/год, - годовая паропроизводительность
котла;
, т/год, - годовая паропроизводительность
котла; ![]() , т/ч, - расход питательной воды на пуск
котла;
, т/ч, - расход питательной воды на пуск
котла; ![]() , т/ч, - расход питательной воды на
останов;
, т/ч, - расход питательной воды на
останов; ![]() - количество пусков и остановов за год (как
минимум 2);
- количество пусков и остановов за год (как
минимум 2); ![]() - допустимые концентрации гидразина в
питательной воде во время пусков (300мкг/кг) и остановов (1000
мкг/кг) соответственно ; 24 – продолжительность пускового режима.
- допустимые концентрации гидразина в
питательной воде во время пусков (300мкг/кг) и остановов (1000
мкг/кг) соответственно ; 24 – продолжительность пускового режима.
Гидразинную обработку питательной воды ведут непрерывно; рабочий раствор, как правило, вводят после деаэраторов, во всасывающий трубопровод питательного насоса. Процесс регулируется автоматически по импульсу от расхода питательной воды.
8.1.2 Фосфатный водный режим
С целью предотвращения образования в котлах твёрдой кальциевой накипи ведут фосфатную обработку котловой воды. Фосфатный режим является надёжным средством предотвращения кальциевого накипеобразования и не должен рассматриваться как способ исключения накипеобразования вообще.
В результате взаимодействия ионов РО43- с ионами Са2+ образуется гидроксилаппатит [ Са(Са3(РО4)2)3] × (ОН)2 в виде тончайшей взвеси (шлама). В отличие от гидроксилаппатита в котловой воде возможно образование фосфорита Са3(РО4)2, который выделяется на поверхности металла в виде твёрдой накипи. Условия образования указанных соединений различны и определяются значением рН среды.
Образование фосфорита отмечается в питательном тракте и экономайзере при относительно низких значениях рН в сравнении с котловой водой, а образование гидроксилаппатита происходит в щелочной среде котловой воды. Этим обстоятельством и определены оптимальные условия ввода раствора фосфата не в питательную, а непосредственно в котловую воду.
Действие фосфата натрия на процесс кальциевого накипеобразования можно объяснить следующим образом: при избытке в котловой воде ионов РО43- образуется малорастворимое соединение и концентрация ионов кальция снижается настолько, что котловая вода не достигает состояния насыщения по отношению к таким накипеобразователям, как СаSiO3, СаSO4 и т.д. В результате весь кальций, поступающий в котловую воду, осаждается в ней в виде гидроксилаппатита в форме шлама.
В связи со сложным составом котловой воды, содержащей наряду с катионами Са2+, Мg2+, Fe3+ и анионы СО32-, SO42-, SiO32-, расчёт потребной концентрации ионов для фосфатной обработки выполнить практически невозможно. В котловой воде должна быть достаточная щёлочность, чтобы происходило образование гидроксилапатита, и в то же время не должно быть большого избытка РО43-, чтобы избежать образования твёрдой накипи Мg3(РО4)2 и фосфата железа.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.