 |
 |
|||
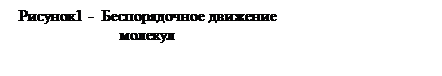 |
|||
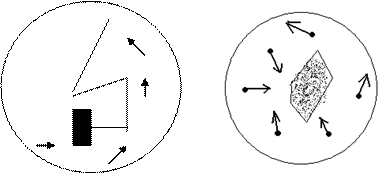
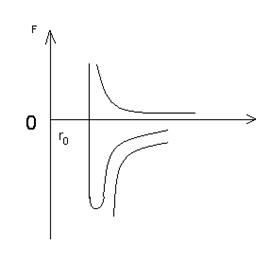
Проанализируем взаимодействие молекул, которые для простоты примем в виде одиночных атомов. При сближении атомов их электронные оболочки будут деформироваться и в этом случае атомы можно представить как диполи, следовательно, любые две молекулы должны при взаимодействии проявлять и взаимодействие и отталкивание. Природа взаимодействия молекул электрическая. Обычно молекулярные силы изображаются графически. Как показывают расчеты, кривые притяжения и отталкивания несколько отличаются друг от друга. Кривая отталкивания круто опускается к оси ОR и лежит ближе к оси ОF, чем кривая сил притяжения. Результирующая сила изображается довольно сложной кривой, с ясно выраженной впадиной в области сил притяжения. При r = r0 силы притяжения уравновешены силами отталкивания и Fр = 0. Если r < r0, то преобладают силы отталкивания, причем Fр может достигать больших величин. При r > rо будут преобладать силы притяжения, при этом Fр увеличивается до определенного предела, после чего Fр уменьшается и стремится к нулю - происходит разрыв между молекулами (см. рисунок 2).
Энергии молекулярного взаимодействия
 Взаимодействие молекул, как и любых других физических
объектов, характеризуется не только силой, но и энергией взаимодействия.
Графики энергии взаимодействия молекул - диполей ведут себя в какой-то мере
аналогично графикам сил взаимодействия. При r=r0 энергия
взаимодействия молекул минимальная Wm. При г > r0 и r
< r0 энергия взаимодействия увеличивается, при чем r < r0 энергия увеличивается до очень больших величин, а при
r > r0 - до определенного предела W0.
Как известно, нулевой уровень потенциальной энергии может быть выбран произвольно.
Удобно предположить, что потенциальная энергия равна нулю при бесконечном
удалении молекул друг от друга. Тогда при r> r0 она
Взаимодействие молекул, как и любых других физических
объектов, характеризуется не только силой, но и энергией взаимодействия.
Графики энергии взаимодействия молекул - диполей ведут себя в какой-то мере
аналогично графикам сил взаимодействия. При r=r0 энергия
взаимодействия молекул минимальная Wm. При г > r0 и r
< r0 энергия взаимодействия увеличивается, при чем r < r0 энергия увеличивается до очень больших величин, а при
r > r0 - до определенного предела W0.
Как известно, нулевой уровень потенциальной энергии может быть выбран произвольно.
Удобно предположить, что потенциальная энергия равна нулю при бесконечном
удалении молекул друг от друга. Тогда при r> r0 она
равна нулю: происходит
разрыв молекулярных связей. Максимальная энергия взаимодействия W![]() зависит от рода материала. Если молекуле
сообщить некоторую энергию W1, то она начинает совершать колебания,
при которых потенциальная энергия превращается в кинетическую и наоборот, а
уровень полной энергии остается неизменным (см. рисунок 3).
зависит от рода материала. Если молекуле
сообщить некоторую энергию W1, то она начинает совершать колебания,
при которых потенциальная энергия превращается в кинетическую и наоборот, а
уровень полной энергии остается неизменным (см. рисунок 3).
Внутренняя энергия. Полная энергия
Работа. Теплообмен. Первое начало термодинамики
Тела состоят из частиц. Частицы находятся в движении и взаимодействии, следовательно, они обладают кинетической и потенциальной энергией. Под частицами в узком смысле понимают молекулы, в широком - все частицы, включая и внутриатомные.
Полную энергию тела можно разделить на внешнюю и внутреннюю энергию. Внешняя энергия включает в себя энергию движения тела и энергию его взаимодействия, как целого с другими физическими объектами. Остальная часть полной энергии называется внутренней энергией тела.
Таким
образом, ![]()
где U- внутренняя энергия тела, а N- число молекул тела.
Внутренняя энергия, как и другая, может изменяться. Существует два способа изменения внутренней энергии.
1 Внутренняя энергия может изменяться за счет других видов энергии (электрической, механической и т.д.). Следует отметить, что в этом случае наблюдается взаимное превращение внутренней и других видов энергии. Считается, что изменение энергии с превращением её в другие виды определяется работой. Значит, при этом способе изменение внутренней энергии совершается работа:
ΔU=ΔWмех→ΔU=Aмех
ΔU=ΔWэл→ΔU=Аэл
Известно, что при ударах молота, резании, сверлении, при пропускании электрического тока тела нагреваются.
2 Внутренняя энергия средних тел может изменяться за счет внутренней энергии других тел. В этом случае энергия без превращения передается от одних тел к другим, то есть, работа не совершается. Этот случай изменения внутренней энергии называют теплообменом. Количество внутренней энергии отданной или полученной при теплообмене, называют количеством теплоты.
ΔU=Q,
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.