1 Объясните формулу Е=3/2КТ и ее физический смысл. Дайте определение температуры на основе этой формулы. Из данной формулы можно получить важные следствия:
а) среднее значение кинетической энергии поступательного движения молекул (Е) не зависит от природы газа, а определяется только его температурой (Т);
б) при одинаковой температуре средние квадратичные скорости
движения молекул (V) обратно пропорциональны корню квадратному из масс молекул. Докажите это.
2 Два газа (кислород и водород) имеют одинаковую температуру. С одинаковой ли средней квадратичной скоростью движутся молекулы этих газов? Одинакова ли их кинетическая энергия? Можно ли говорить о температуре одной или нескольких молекул?
3Определите среднюю кинетическую энергию поступательного движения молекулы газа при температуре 1500С.
4 Может ли газ при температуре - 40ºС иметь среднюю кинетическую энергию поступательного движения молекулы, равную 4,6* 10-21 Дж?
5 Какова средняя квадратичная скорость атома водорода в атмосфере Солнца при температуре 6000 К?
6 Газ в цилиндре изотермически сжали. Объясните, используя уравнение, почему давление газа увеличивается.
7 В закрытом цилиндре нагревают газ. Почему при этом изменяется давление газа? Изменяется ли концентрация молекул газа?
1 группа
1 Какова масса 50 молей углекислого газа?
2 При автогенной сварке используют сжатый кислород, который хранится в баллонах емкостью 20 л. При 17º давление в баллонах 100 атм. Какой объем займет газ при нормальных условиях?
3 Имеется 12 л углекислого газа под давлением 9 • 105 Па и температуре 288 К. Определить массу газа (0,2 кг).
4 Баллон вместимостью 40 л содержит кислород массой 2,6 кг. При какой температуре возникнет опасность взрыва, если допустимое давление не более 50 • 103 Па (296 К).
5 Какая линия на графике соответствует большему объему:
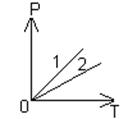
6 Сколько молекул воздуха содержится в комнате объемом 60 и при нормальных условиях? µ=29 кг/к моль
7 Газ при давлении 3,2*10 Па и температуре 17 ºС занимает объем 87 л. Привести объем газа к нормальным условиям.
8 Вычислить молярную массу бутана, 2 л которого при температуре 15°С и давлении 9*104 Па имеют массу 4,2 г (56 кг/кмоль).
9 В баллоне емкостью 12 л находится водород массой 100 г под давлением 9.8*106 Па. Какова температура этого газа (10 С).
10 Перечертите графики в координатах Р(Т) и V(Т):
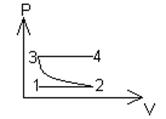
11 При нормальных условиях масса газа 738,6 мг, а объем 8,205 л. Какой это газ?
12 Определить плотность водорода при температуре 15º С и давлении 730 мм. рт. ст. (0,0811 кг/м3).
13 Б батискафе содержится воздух массой 4,2 кг при давлении 10 Па и температуре 17° С. На сколько времени хватит этого воздуха человеку, если в минуту он потребляет 750 куб. см воздуха? μ=29 кг/кмоль (77 часов).
14 Масса 14,92*1025 молекул инертного газа составляет 5 кг. Какой это газ?
15 Перечертите график в координатах P(T) и P(V)
![]() V 3
V 3![]()
2
![]()
![]()
|
T
2 группа
1 Определить массу 20 л аммиака (NНз), находящегося под давлением 1450 мм. рт. ст. и температуре 17°С (28 г).
2 Объем пузырька газа, всплывшего со дна озера на поверхность, увеличился в 3 раза. Какова глубина озера? Атмосферное давление нормальное, температура не изменится (20 м).
3 В баллоне объемом 0,2 м3 находится гелий под давлением 105 Па и температуре 17°С. После накачивания гелия его давление увеличилось в 3 раза, а температура до 47°. Найти изменение массы гелия (57 г).
4 Какой объем занимают 100 молей ртути ( 1 ,5 л)?
5 Какая температура больше Т1 или Т2
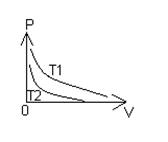
6 Газ находится под поршнем площадью 10 см2 в горизонтальном цилиндрическом сосуде. Объем газа 50 л. С какой силой надо действовать на поршень, чтобы объем газа стал 10 л?
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.