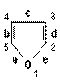
 Пример. В фурановом
кольце принята следующая нумерация атомов и связей:
Пример. В фурановом
кольце принята следующая нумерация атомов и связей:
![]()
![]() Присоединение
бензольного кольца к фурановому возможно по связям «b» и «c» с образованием
бенз[b]фурана и бенз [с] фурана:
Присоединение
бензольного кольца к фурановому возможно по связям «b» и «c» с образованием
бенз[b]фурана и бенз [с] фурана:
бенз[b]фуран бенз[c]фуран
Атомы водорода в гетероциклах обозначаются «адресом» с символом каждого водорода перед названием гетероцикла, например:
![]()
![]()
![]()
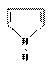
пиррол 2H-пиррол бенз[b]пиррол 6H-бенз[b]пиррол
Приложение 7.
Высокомолекулярные соединения
|
|
инициирование |
|
|
рост цепи |
|
|
обрыв цепи |
Этот тип полимеризации называется радикальным.
Полимеризация может инициироваться катионами или анионами (ионами).
Катионная полимеризация:
|
|
|
|
|
и т. д. |
Инициаторами катионной полимеризации могут быть H+, неорганические апротонные кислоты SnCl4, AlCl3, металлоорганические соединения Al(C2H5)3.
|
|
|
|
|
|
|
|
рост цепи |
|
|
обрыв цепи |
Анионная полимеризация:
Инициаторами анионной полимеризации обычно служат электронодонорные соединения (щелочные металлы, их алкоголяты и т. д.).
Сополимеризация - полимеризация между разными мономерами.
Примеры полимеров и сополимеров, получаемых реакцией полимеризации.
|
Мономер |
Мономерное звено |
Полимер |
|
этилен |
|
полиэтилен |
|
винилхлорид |
|
поливинилхлорид |
|
стирол |
|
полистирол |
|
бутадиен-1,3 |
|
полибутадиен |
|
стирол + бутадиен-1,3 |
|
полистиролбутадиен |
Поликонденсация сопровождается образованием полимера и низкомоле-кулярного соединения (H2O, HCl, NH3 и т. п.). Мономеры должны содер-жать минимум две функциональные группы.
Реакция поликонденсации лежит в основе получения фенолформальдегидных смол и полиэфирных соединений.
Примеры полимеров, получаемых реакцией поликонденсации:
|
Мономеры |
Полимер |
Название |
Полимер |
Название |
|
|
|
полиэфир |
[-SiR2-O-]2 |
полисилоксаны |
|
|
|
фенолоформальдегид-ные смолы |
[-(OC)C6H4(CO)OCH2CH2-]n |
полиэтилентерефталат |
|
|
|
полиангидрид |
[-OROCONHR/NHCO -]n |
полиуретаны |
|
|
|
поликарбамид |
[-OROCHR/ -] |
полиацетали |
Оглавление стр.
Методические указания по изучению дисциплины. Рабочая программа. …...3
Раздел I. Основы теории строения органических соединений………………..6
Тема 1. Строение молекул органических веществ…….……………………...7
Тема 2. Основные понятия……………………………………………………..8
Тема 3. Пространственное расположение атомов и геометрия молекул..….10
Тема 4. Пространственные эффекты………………………………………….11
Тема 5. Электронные эффекты………………………………………………...11
Тема 6. Типы органических реакций………………………………………....13
Тема 7. Механизмы органических реакций………………………………….14
Раздел II. Углеводороды………………………………………………………...17
Тема 1. Алканы. Циклоалканы………………………………………………...17
Тема 2. Алкены (Олефины)…………………………………………………….21
Тема 3. Алкины (Ацетиленовые углеводороды)…………………………….24
Тема 4. Алкадиены……………………………………………………………..27
Тема 5.Арены (Ароматические углеводороды)……………………………....30
Тема 6.Природные источники углеводородов.Переработка углеводородов.34
Тема 7. Галогенуглеводороды…………………………………………………36
Раздел III. Кислородсодержащие органические соединения…………………40
Тема 1. Спирты и фенолы. Простые эфиры…………………………………..41
Тема 2. Альдегиды и кетоны…………………………………………………..45
Тема 3. Карбоновые кислоты………………………………………………….48
Тема 4. Сложные эфиры. Жиры……………………………………………….53
Тема 5. Углеводы……………………………………………………………….55
Раздел IV. Азотсодержащие органические соединения………………………59
Тема 1. Амины……………………………...…………………………………..60
Тема 2. Аминокислоты. Белки……………….………………………………..62
Тема 3. Нитросоединения…..………………………………………………….65
Раздел V. Гетероциклические органические соединения……………………..68
Общие вопросы к разделу ГЦС………………………………………………..68
Тема 1.Азотсодержащие ГЦС…..………...…………………………………...69
Тема 2. Кислородсодержащие ГЦС…..…...…………………………………..71
Тема 3. Серосодержащие ГЦС…..………...…………………………………..73
Раздел VI. Высокомолекулярные соединения………………………………...76
Тема 1.Основные определения …..………...………………………………....77
Тема 2. Строение макромолекул…..…...……………………………………...78
Тема 3. Отличительные свойства полимеров………………………………...79
Тема 4. Способы образования полимеров.…………………………………...79
Тема 5. Природные полимеры………………….……………………………..80
Тема 6. Химические волокна ……...…………………………………..81
Тема 7. Пластические массы..…..………...…………………………………...81
Тема 8. Элементорганические полимеры....…………………………………..81
Тема 9. Синтетические смолы…..………...…………………………………...81
Задание по расчетно – графической работе……………………………………83
Список рекомендуемой литературы……………………………………………85
Приложение………………………………………………………………………86
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.