Результатами расчета блока синтеза аммиака являются выработка аммиака и необходимая мощность компрессора.
Перейдем к рассмотрению блока синтеза метанола. Материальный баланс стадии конденсации воды (см. рис. 8) сводится решением уравнения (2.38), стадии конденсации метанола-сырца – решением методом итераций системы из двух уравнений типа (2.31), записанных для двух веществ – метанола и воды. Материальный баланс стадии синтеза метанола вытекает из расчета реактора по методике, изложенной в разделе 2.4.4.
Тепловой баланс реактора выразили уравнением:
Q1 + Q2 = Q3 + Q4 (2.71)
где Q1 - физическое тепло газовой смеси на входе в реактор; Q2 - тепловые эффекты реакций (2.22),(2.23); Q3 - физическое тепло газовой смеси на выходе из реактора; Q4 - тепло, подлежащее утилизации. Количество выработанного пара G (кг/ч), находили по формуле:
G = Q4/(Нп – Нв) (2.72)
где Нп и Нв – энтальпии пара на выходе из реактора и воды на входе в реактор, Дж/кг.
В Главе 4 мы рассмотрим вопросы организации теплообмена в контуре метанола. Независимо от способа организации схема теплообмена будет включать набор аппаратов, для которых характерны типичные уравнения теплового баланса. На рис. 11 условно изображен теплообменный аппарат.
|
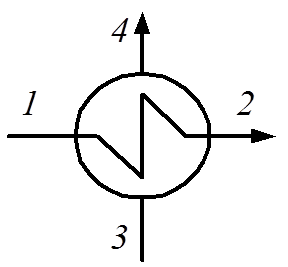
Рис. 11. Схема элемента с теплообменом 1,2,3,4 – потоки |
Пусть в результате охлаждения потока 1-2 из него конденсируется жидкая фаза. Тогда уравнение теплового баланса записывали следующим образом:
Q1 + Q2 = Q3 + Q4 (2.73)
где Q1 – теплота охлаждения сухого газа потока 1-2; Q2 – теплота охлаждения и фазового перехода конденсирующихся компонентов потока 1-2; Q3 – теплота нагрева потока 3-4, Q4 - потери тепла.
Во всех рассматриваемых случаях известны состав и температура потоков 1 и 3. Если неизвестная величина - температура потока 4, то ее находили из уравнения (2.73). Так как для вычисления энтальпии потока 4 нужно заранее знать температуру потока, то уравнение (2.73) решается итерационным методом.
Если неизвестны температура и состав потока 2, то уравнение (2.73) записывали совместно с уравнениями материального баланса (2.31) или (2.38). Полученную систему уравнений решали итерационными методами, т.к. температура, состав и энтальпия потока 2 взаимозависимы.
Если в аппарате не происходит никаких фазовых переходов, то тепловой баланс выражали простым уравнением:
Q1 + Q2 = Q3 + Q4 + Q5 (2.74)
где Q1,Q2,Q3,Q4 - энтальпии соответствующих потоков; Q5 – потери тепла.
В главе 4 мы будем рассматривать возможность применения огневого подогревателя для перегрева пара, вырабатываемого в реакторе синтеза метанола. Тепловой баланс подогревателя записывали следующим образом:
Q1 + Q2 + Q3 + Q4 = Q5 + Q6 (2.75)
где Q1 - физическое тепло насыщенного пара на входе; Q2 - физическое тепло топливного природного газа на входе; Q3 - физическое тепло воздуха (для горения) на входе; Q4 - теплота реакций горения природного газа; Q5 - физическое тепло перегретого пара на выходе; Q6 - физическое тепло дымовых газов на выходе. Из уравнения (2.75) находили необходимый расход топливного природного газа.
2.6. Моделирование схем с рециркулирующими потоками.
Как было показано выше (см. рис. 8,10), блоки синтеза метанола и аммиака имеют рециркулирующие потоки. Моделирование структуры ХТЭС, имеющей рециркулирующие материальные потоки - весьма сложная задача, т.к. приходиться применять итерационные методы. Представленная здесь методика моделирования описана в [19].
|
Рис. 12. Структура ХТЭС с рециклом |
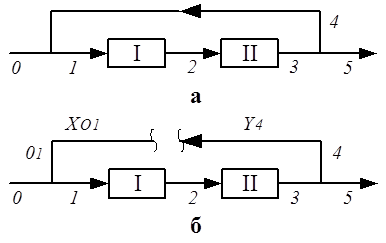 Структура ХТЭС с
рециклом условно представлена на рис. 12а. Состояние потока на входе в элемент I зависит от входного потока 0
и состояния потока 4 после ответвления его от потока 3 за
элементом II. Чтобы рассчитать элемент I, нужно уже знать результат расчета
элемента II, что невозможно. Поэтому разрывают
связи рецикла, как показано на рис. 12б. Структура становится линейной с
неизвестным состоянием Х01 входного потока 01.
Задают какие-то параметры его состояния и рассчитывают полученную линейную структуру.
По окончании расчета состояния потоков 01 и 4 должны
совпадать, в противном случае задают новые значения Х01 и
повторяют расчет до указанного совпадения. Конечно, добиться точного равенства Х01
= Y4 невозможно, поэтому стараются минимизировать разность
между ними:
Структура ХТЭС с
рециклом условно представлена на рис. 12а. Состояние потока на входе в элемент I зависит от входного потока 0
и состояния потока 4 после ответвления его от потока 3 за
элементом II. Чтобы рассчитать элемент I, нужно уже знать результат расчета
элемента II, что невозможно. Поэтому разрывают
связи рецикла, как показано на рис. 12б. Структура становится линейной с
неизвестным состоянием Х01 входного потока 01.
Задают какие-то параметры его состояния и рассчитывают полученную линейную структуру.
По окончании расчета состояния потоков 01 и 4 должны
совпадать, в противном случае задают новые значения Х01 и
повторяют расчет до указанного совпадения. Конечно, добиться точного равенства Х01
= Y4 невозможно, поэтому стараются минимизировать разность
между ними:
D = ½Х01 – Y4½< e
где e - точность расчета.
Мы полагаем, что точность расчета удобнее оценивать не по разностям, как в описанной выше методике, а по соотношениям вида:
e = Х01/ Y4
Очевидно, что e должно быть равно 1,0 с какой-либо заданной точностью.
На рис. 13 показана структурная схема блока синтеза метанола. На схеме показана точка ''разрыва'' ХТЭС.
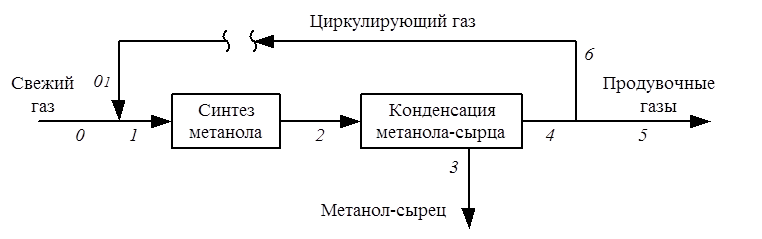
Рис. 13. Структурная схема контура метанола-сырца.
В балансовых расчетах мы пренебрегли растворимостью газов в жидкой фазе ввиду их малого количества – по проверочному расчету не более 0,1 % от общего количества циркулирующего газа.
Объем циркулирующего газа должен быть фиксирован:
Vцирк = K×Vисх (2.76)
где K – кратность циркуляции; Vисх – объем исходного (свежего) газа.
Модель не накладывает никаких ограничений на объем продувочных газов (конечно, он не может быть отрицательным), т.к. они возвращаются в агрегат аммиака.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.