Английские ученые Джоуль и Томсон в 1852÷1862 г.г. обнаружили и изучили явление изменения температуры при прохождении газа через дроссель. Это явление названо эффектом Джоуля-Томсона. Эффект Джоуля-Томсона называется положительным, если газ в процессе дросселирования охлаждается (∆Т<0), отрицательным, если газ нагревается (∆Т>0).
Дросселирование, как термодинамический процесс, характеризуется постоянством энтальпии, т.е. изоэнтальпийный процесс i=const.
Эффект Джоуля-Томсона согласно молекулярно-кинетической теории можно пояснить межмолекулярным взаимодействием, т.е. внутренней энергией системы. Последняя имеет две составляющие: потенциальную и кинетическую. Расширение газа в условиях изоляции не меняет ее внутренней энергии, но приводит к росту потенциальной энергии за счет уменьшения кинетической энергии, которая определяется тепловым движением молекул, т.е. приводит к снижению температуры.
В действительности, эффект Джоуля-Томсона сложнее, так как газ не изолирован энергетически от внешней среды, он совершает внешнюю работу, последующие порции газа теснят после дросселя предыдущие порции. В адиабатических условиях эта работа идет на изменение внутренней энергии. Зная состояние состояния, изменение давления, выражение для внутренней энергии, можно найти изменение температуры.
Коэффициент, определяемый как изменение температуры при изменении давления на единицу, называется коэффициентом Джоуля-Томсона.
В соответствии с эффектом Джоуля-Томсона он может быть положительным, отрицательным, равным нулю. Температура, при которой для данного давления изменение ее равно нулю, называется температурой инверсии. Таким образом, коэффициент Джоуля-Томсона Di определяется, как Di=∆Т/∆Р.
В практике газовой технологии для расчета используют, например, энтальпийные диаграммы (см. рисунок 2.6.1).
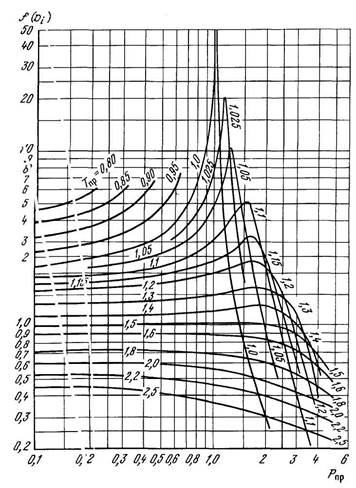
Рисунок 2.6.1 – Зависимость обобщенной функции f(Di) от приведенных давления и температуры.
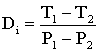 (2.6.1)
(2.6.1)
Полученную Гухманом и Нагаревой зависимость вида:
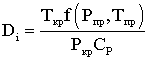 (2.6.2)
(2.6.2)
![]() (2.6.3)
(2.6.3)
при 1,6≤Тпр≤2,1 и 0,8≤Рпр≤3,5
Для более точного определения коэффициента Джоуля-Томсона необходимо использовать соответствующие условиям уравнения состояния.
Например, для реальных природных газов коэффициент Джоуля-Томсона записывается в виде:
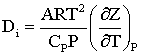 (2.6.4)
(2.6.4)
Частную производную 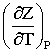 можно найти из уравнения
состояния Пенга-Робинсона:
можно найти из уравнения
состояния Пенга-Робинсона:
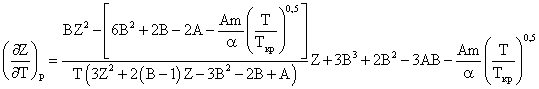 (2.6.5)
(2.6.5)
Среднее значение коэффициента Джоуля-Томсона для природного газа изменяется от 2 до 4 К/МПа.
2.7. Влагосодержание природных газов.
При эксплуатации газовых и газоконденсатных месторождений газы в пластовых условиях контактируют с остаточной, пластовой или подошвенной водами и насыщаются парами воды. Количество паров воды зависит от температуры и давления, а также от состава газа, степени минерализации пластовой воды. Главенствующими являются температура и давление.
Влагосодержание природных газов – один из факторов, определяющих технологию добычи и подготовки продукции скважин для дальнейшего транспорта или использования. Различают абсолютную и относительную влажности. Под абсолютной влажностью газа понимается количество водяных паров, выраженных в массовых единицах, которое фактически находится в единицах объема или массы газа. В первом случае единицей измерения является г/м3 при 293 К и 0,1013 МПа (или кг/1000 м3), во втором – г/кг газа. В промысловой практике чаще используют – кг/1000 м3 при 293 К и 0,1013 МПа.
Относительная влажность – это отношение абсолютной влажности к максимально возможному влагосодержанию при данных давлении и температуре, она выражается в долях единицах или процентах.
Одной из характеристик газа, учитывающая ее влагосодержание, является точка росы по влаге, которая равна температуре конденсации паров воды.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.