Следует отметить, что в области давлений до 5 МПа и при давлениях схождения больше 25 МПа (условия близкие к промысловой сепарации и стабилизации конденсата) влиянием давления схождения на константы равновесия можно пренебречь, т.е. аппроксимационные зависимости определяются только давлением и температурой.
Константы равновесия углекислого газа и сероводорода определяются по следующим формулам
![]() (2.9.18)
(2.9.18)
![]() –
определяются изложенным выше способом;
–
определяются изложенным выше способом;
![]() (2.9.19)
(2.9.19)
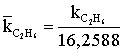 ;
;
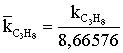
а1=0,0016766885; а2=0,98323311; а3=1,0331174; а4= –0,0008977.
Константу равновесия остатка kс7+, или kс6+, или kс5+.
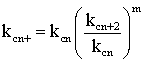 (2.9.20)
(2.9.20)
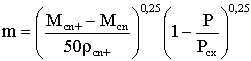 (2.9.21)
(2.9.21)
где n≥5.
Константы фазового равновесия могут быть определены с использованием уравнения состояния. Уравнение состояния реальных газов позволяет найти летучести компонентов в газовой и жидкой фазах, константа равновесия может быть рассчитана как отношение летучести компонента в газовой фазе к летучести в жидкой фазе.
Понятие летучести для расчетов фазовых переходов введено Льюисом. Летучесть есть “исправленная” упругость насыщенных паров компонентов идеальных растворов или “исправленное” парциальное давление компонентов идеальных газовых смесей.
Летучесть f представляет собой “исправленное” давление, при подстановки которого в уравнения идеальных газов или растворов они становятся пригодными для описания свойств реальных газов или растворов, при этом летучесть для каждого реального газа определяется экспериментально при различных давлениях и температурах.
Для идеального
однокомпонентного газа летучесть f равна давлению Р, для смеси газов – парциальному давлению i-го компонента ![]() .
.
Для реальных газов летучесть и коэффициент сверхсжимаемости имеют следующее соотношение
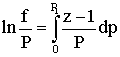 (2.9.22)
(2.9.22)
или приближенно можно записать
![]() (2.9.23)
(2.9.23)
Отношение fiг к уiР называется коэффициентом летучести ψi, т.е.
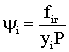 (2.9.24)
(2.9.24)
где fiг – летучесть i-го компонента в газовой фазе; уi – мольная доля i-го компонента в газовой фазе.
Коэффициент активности γi есть отношение fiж к хifiж0, следовательно:
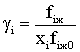 (2.9.25)
(2.9.25)
где fiж – летучесть i-го компонента в жидкой фазе; fiж0 – летучесть чистого компонента при температуре смеси; хi – мольная доля i-го компонента в жидкой фазе.
При термобарическом равновесии летучести в газовой и жидкой фазах равны, т.е. fiг=fiж, отсюда:
![]()
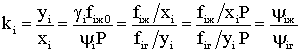 (2.9.26)
(2.9.26)
Значения коэффициентов сверхсжимаемости для газовой zg и жидкой фаз z1 определяются по следующим уравнениям:
![]() (2.9.27)
(2.9.27)
![]() (2.9.28)
(2.9.28)
где: ![]() (2.9.29)
(2.9.29)
![]() (2.9.30)
(2.9.30)
![]() (2.9.31)
(2.9.31)
![]() (2.9.32)
(2.9.32)
![]() (2.9.33)
(2.9.33)
![]() (2.9.34)
(2.9.34)
индексы g – газовая фаза; 1 – жидкая фаза; i – число компонентов в газовой и жидкой фазах.
![]() (2.9.35)
(2.9.35)
![]() (2.9.36)
(2.9.36)
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.