· хлорангидриды > ангидриды > карбоновые кислоты.
· метанол > первичный > вторичный > третичный спирт
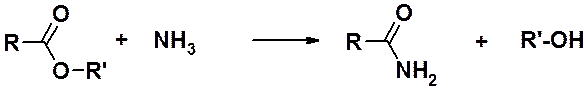
Аммонолиз сложных эфиров
Аммонолиз похож на реакции гидролиза и переэтерификации. В качестве нуклеофила, замещающего спиртовый фрагмент, используют аммиак, амиды щелочных и щелочноземельных металлов.
Каталитическое восстановление сложных эфиров протекает в присутствии медного катализатора при высоких температуре и давлении. Результатом всегда являются первичные спирты.
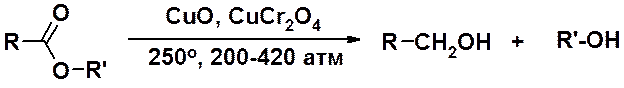
Восстановление до первичных спиртов может быть проведено также комплексными гидридами металлов или натрием в спирте.
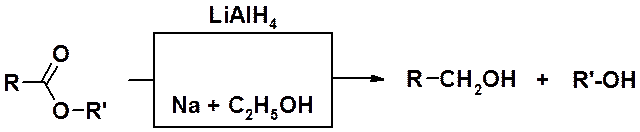
СН-кислотность a-водородов сложноэфирной группы, является фактором обусловливающим возможность протекания конденсации в присутствии сильных оснований. Результат реакции – эфиры b-кетокислот.
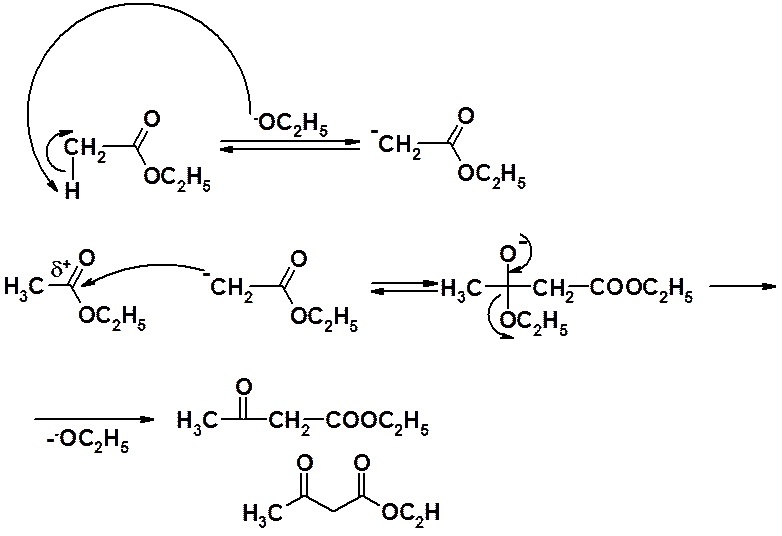
· Амиды. Получение: ацилирование аммиака и аминов. Химические свойства: амидное сопряжение, кислотно-основные свойства (сравнить с аминами), восстановление, перегруппировка Гофмана, алкилирование.
Общая формула амидов:
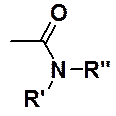
Если:
· R’ и R” атомы водорода – незамещенные амиды;
· R’ – водород, R” – углеводородный радикал - монозамещенные амиды;
· R’ и R” - углеводородные радикалы - дизамещенные амиды.
Практическое значение имеют, в первую очередь, незамещенные и монозамещенные амиды.
Наиболее общие метод получения амидов (от незамещенных до дизамещенных) – ацилирование (введение ацильной группы) аммиака и его производных (аминов).
Простейший, на первый взгляд, и ошибочный метод – получение амида взаимодействием карбоновой кислоты с аммиаком.
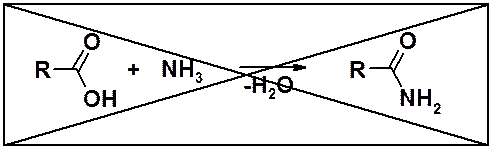
Следует помнить о кислотно-основных свойствах реагирующих веществ. Реакция получения амидов – нуклеофильное замещение ОН-группы. Взаимодействие кислоты с аммиаком приводит к аммонийным солям.
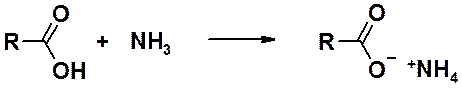
Карбоксилат-анион – частица с избытком электронной плотности, для которой реакция с нуклеофилами затруднена, если не невозможна.
В некоторых случаях аммонийная соль может быть превращена в амид нагреванием при температуре > 200о.
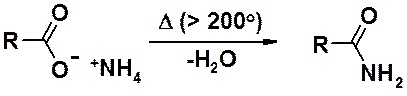
Реакция применима только для простейших кислот с углеводородным радикалом. Соединения, имеющие в углеводородной части молекулы функциональные группы обычно разлагаются при более низких температурах, чем необходимо для отщепления воды.
Гладко протекаю реакции ацилирования аммиака и аминов ангидридами и хлорангидридами кислот.
Ацилирование аммиака и его производных ангидридами
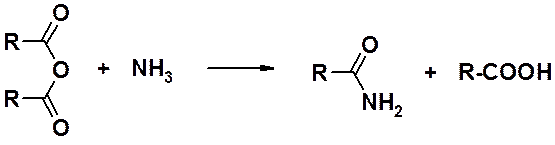
Недостатком этого метода является большой расход карбоновой кислоты, т.к. половина молекулы ангидрида расходуется впустую.
Ацилирование аммиака и его производных хлорангидридами
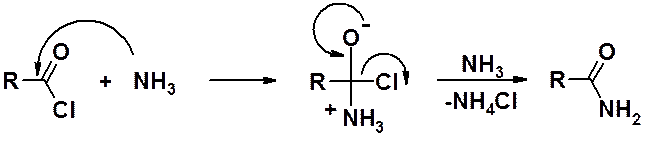
В реакции всегда используют двойной избыток аммиака: одна молекула для введения амидной группы, вторая – для связывания хлористого водорода.
Незамещенные амиды могут быть получены частичным гидролизом нитрилов.
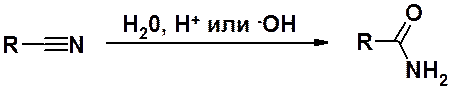
В отличие от большинства производных аммиака, проявляющих сильно основные свойства, амиды амфотерные соединения.
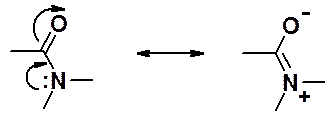
Сопряжение неподеленной пары электронов амидного азота с карбонильной группой, приводит к сдвигу электронной плотности в сторону кислорода. Связь C-N имеет частично двойной характер, ее длина (1,32 Å) заметно меньше длины одинарной C-N связи (1,47 Å).
В реакциях с сильными основаниями амиды проявляют кислые свойства. Кислотность амидов близка к кислотности спиртов (рКа 15-19). Кислотные свойства используют в реакциях алкилирования.
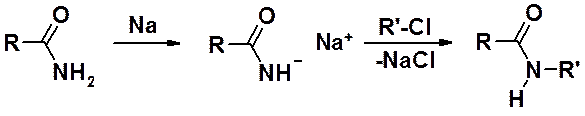
Основность амидов также низка. Только в реакциях с сильными кислотами происходит протонирование, причем оно проходит по атому кислорода.

Восстановление незамещенных амидов комплексными гидридами щелочных металлов (LiAlH4) приводит к первичным аминам, а - моно- и дизамещенных соответственно к вторичным и третичным аминам.
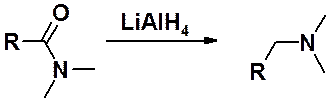
При восстановлении металлическим натрием в жидком аммиаке в присутствии этанола образуются альдегиды.
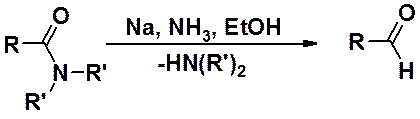
Кислотный гидролиз приводит к карбоновой кислоте и аммонийной соли.
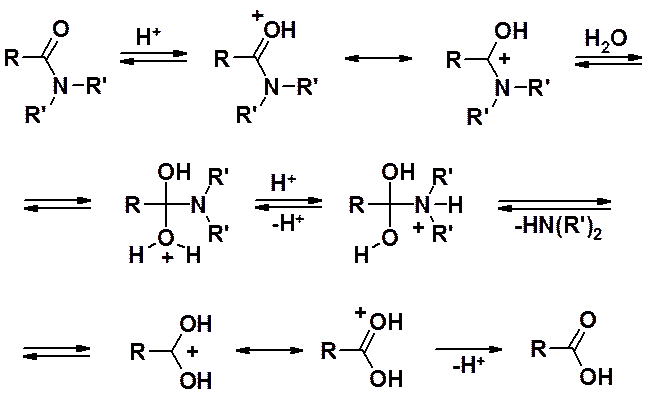
В результате щелочного гидролиза образуется соль кислоты и амин или аммиак.
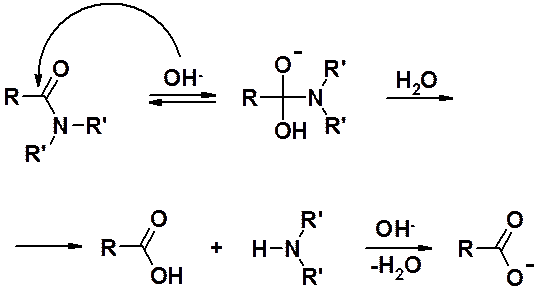
Бромирование незамещенных амидов в щелочной среде ведёт к образованию первичных аминов.
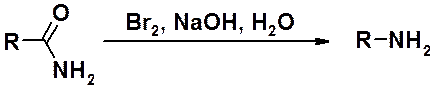
Реакция состоит из нескольких стадий: первоначального образования N-бромамида, который перегруппировывается в изоцианат, гидролиз изоцианата до карбаминовой кислоты и декарбоксилирования последней в амин.
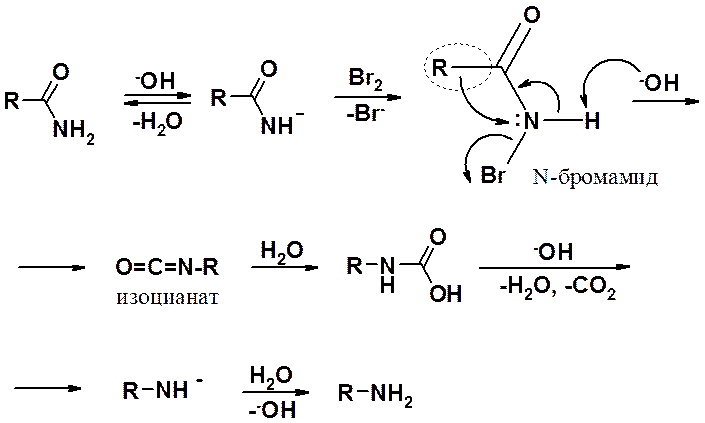
Очень важная особенность перегруппировки Гофмана в том, что она проходит с сохранением конфигурации, т.е. открывает возможность стереонаправленного синтеза. Например, взяв в качестве исходного соединения (+)-карбоновую кислоту и получив из нее (+)-амид, после перегруппировки будет получен (+)-первичный амин.
· Взаимопревращения амидов и нитрилов. Получение нитрилов дегидратацией амидов кислот. Химические свойства: гидролиз, аммонолиз, каталитическое гидрирование, восстановление алюмогидридом лития, использование в синтезе кетонов ароматического ряда.
· Классификация, изомерия, номенклатура.
· Методы получения: гидролиз динитрилов, синтезы с использованием малонового эфира, окислительное расщепление циклоалкенов и циклических кетонов, окисление диолов, альдегидов, окисление диалкилбензолов.
· Химические свойства: кислотность и ее зависимость от взаимного расположения карбоксильных групп, константы кислотности для первого и второго карбоксила. Поведение дикарбоновых кислот при нагревании. Пиролиз кальциевых и ториевых солей. Получение, свойства и применение производных дикарбоновых кислот.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.