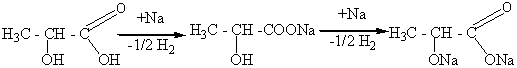
молочная Nа-соль алкоголят молочной
кислота молочной кислоты (и одновре-
кислоты менно соль)
При действии на гидроксикислоты галогенводородов спиртовый гидроксил их молекул замещается на галоген и образуются соответствующие галогенкислоты:

α –гидроксипропионовая α-хлорпропионовая
кислота ( молочная ) кислота
Пятихлористый фосфор замещает на галоген одновременно как спиртовый гидроксил, так и гидроксил карбоксила молекулы гидроксикислот и превращает их таким образом в хлорангидриды хлорорганических кислот:
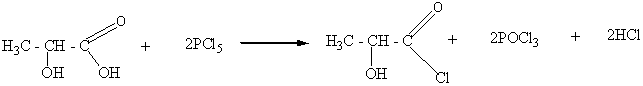 α –гидроксипропионовая
хлорангидрид
α –гидроксипропионовая
хлорангидрид
кислота α –хлорпропионовой
кислоты
При взаимодействии гидроксикислот с диметилсульфатом образуются простые эфиры :
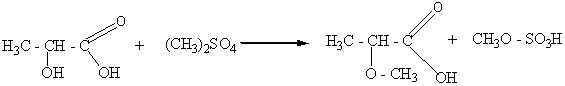
молочная α-метиловый
кислота эфир молочной
кислоты
Гидроксикислоты, как и спирты, могут окисляться. Это свойство гидроксикислот отличает их от карбоновых кислот, которые, как правило, устойчивы к окислению. Гидроксикислоты,которые содержат первичную ОН-группу, при окислении превращаются в альдегидокислоты. А гидроксикислоты с вторичной ОН-группой - в кетокислоты:
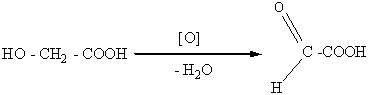
гликолевая глиоксалевая
кислота кислота
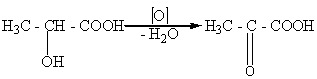
молочная пировиноградная
кислота кислота
Аналогичное окисление молочной кислоты в пировиноградную осуществляется и в живых организмах.
Кроме реакций, которые осуществляются с участием карбоксильной и спиртовой групп, гидроксикислотам свойственны также специфические реакции, обусловленные взаимным влиянием двух функциональных групп в их молекулах. Так, α-, β -,γ-,δ-, и ε -гидроксикислоты по-разному превращаются при нагревании. Гидроксикислоты при повышенных температурах дегидратируются, но в зависимости от взаимного расположения спиртовой и карбоксильной групп дегидратация их происходит по-разному и с образованием разных продуктов реакции.
α-Гидроксикислоты при нагревании отщепляют воду межмолекулярно за счет гидроксила карбоксильной группы одной молекулы гидроксикислоты и атома водорода спиртовой группы другой молекулы гидроксикислоты. Продуктами такой дегидратации являются циклические межмолекулярные сложные эфиры, которые называют лактидами. Так, гликолевая кислота в таких условиях дает кристаллический лактид (2,5-диоксо-1,4-диоксан, или гликолид):
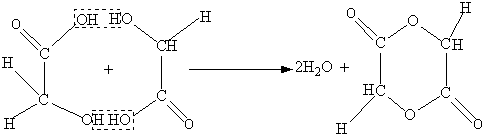
Молочная кислота при дегидратации также образует лактид ( 3,6-диметил-2,5-диоксо-1,4-диоксан):
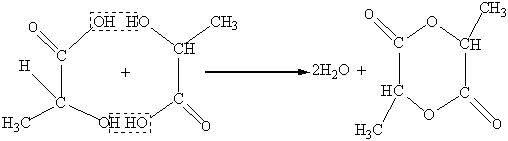
β-Гидроксикислоты при нагревании дегидратируются внутримолекулярно. Вода при этом отщепляется за счет спиртового гидроксила и весьма подвижного α-водородного атома метиленовой группы. В результате образуются α-, β - нередельные кислоты. Так, β-гидроксипропионовая кислота при этом превращается в акриловую кислоту:
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.