ПАСК – кристаллическое вещество (tпл.=147оС), растворяется в большинстве органических растворителей, трудно растворяется в воде, легко декарбоксилируется и превращается при этом в мета-аминофенол.
ПАСК обладает противотуберкулезным действием и применяется в виде натриевой соли. Другие изомеры этой кислоты таким действием не обладают, а м-аминосалициловая кислота, напротив, является высокотоксичным веществом.
Салициловая кислота обладает антиревматическим, жаропонижающим и антигрибковым действием, но, как сильная кислота, вызывает раздражение пищеварительного тракта и поэтому применяется только наружно. Применяется в аналитической химии, медицине, анилинокрасочной и пищевой промышленности, при консервировании фруктов.
Из этой группы кислот наибольшее значение имеет 3,4,5-тригидроксибензойная, или галловая кислота (tпл.=253оС). Кристаллическое вещество, хорошо растворимое в кипящей воде. В природе галловая кислота встречается как свободном, так и в связанном состояниях, обычно в растениях, содержащих дубящие вещества (чернильные орешки дуба, дубовая кора, листья чая). В промышленности галовую кислоту получают гидролизом природного дубильного вещества танина или щелочным плавлением 5-бромпротокатеховой кислоты:
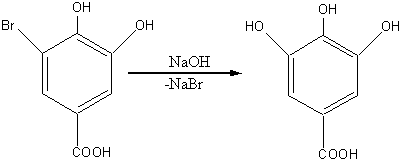
5-бромпротокатеховая кислота галловая кислота
Галловая кислота при нагревании декарбоксилируется и превращается в трехатомный фенол пирогаллол:
|
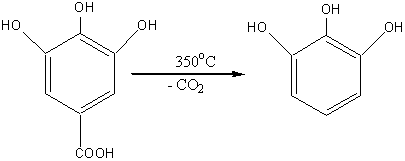
Галловая кислота проявляет сильные восстановительные свойства. Её используют как краситель для приготовления чернила, производные галловой кислоты используются при дублении шкур, в аналитической химии.
Наиболее важной из этого класса кислот является рицинолевая кислота – мононенасыщенная, одноосновная, двухатомная гидроксикислота:
![]()
Является основной кислотой касторового масла (80 –95%). Касторовое масло широко используется в технике в качестве смазывающего вещества, а в медицине как слабительное.
1. Получите молочную кислоту: 1) из пировиноградной кислоты; 2) брожением глюкозы. Что такое асимметрический атом углерода?
2. По какой формуле высчитывают количество оптических изомеров? Напишите оптические изомеры молочной кислоты.
3. Получите винную кислоту. Определите количество асимметрических атомов С*. Напишите все оптические изомеры винной кислоты, назовите их?
4. Получите яблочную кислоту, назовите её по систематической номенклатуре. Напишите её оптические изомеры. Что такое рацемат?
5. Получите двумя способами γ – гидроксимасляную кислоту. Приведите реакции по спиртовой группе.
6. Сравните кислотные свойства молочной и пропионовой кислот; α – гидроксипропионовой и β – гидроксипропионовой кислот.
7. Напишите структурную формулу лимонной кислоты, назовите её по систематической номенклатуре. Обладает ли она оптической изомерией?
8. Сравните отношение α - ,β- и γ – гидроксимаслянных кислот к нагреванию. Назовите полученные соединения.
9. Какие вещества образуются при взаимодействии молочной кислоты с уксусным ангидридом, хлористым водородом?
10. Напишите схемы реакций молочной кислоты с PCl5, этанолом (в присутствии небольшого количества Н3РО4).
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.