![]()
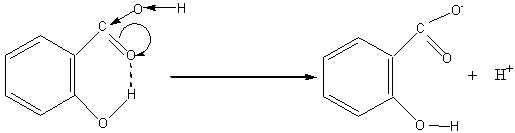
Салициловая кислота способна давать производные по каждой функциональной группе.
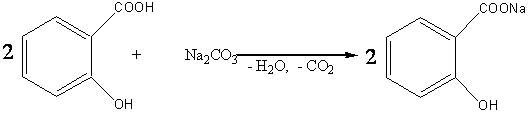
![]()
Со щелочью, в присутствии ее достаточного количества, в реакцию вступает как карбоксильная, так и гидроксильная группа салициловой кислоты:
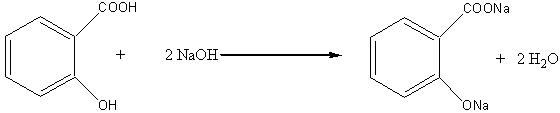
При действии на салициловую кислоту спиртов в присутствии минеральных кислот, например, метилового спирта, образуются сложные эфиры по СООН-группе:
![]()
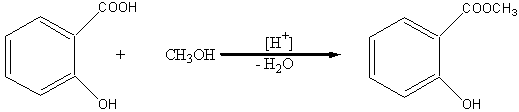
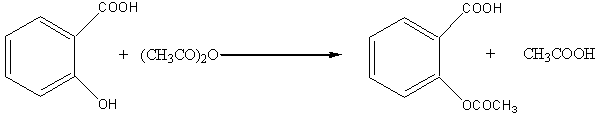
При взаимодействии салициловой кислоты с галогенангидридами или ангидридами кислот в реакцию вступает фенольный гидроксил. В случае ее взаимодействия с ангидридом или хлорангидридом уксусной кислоты образуется ацетилсалициловая кислота (аспирин, tпл.=137оС), который широко используется как жаропонижающий медицинский препарат:
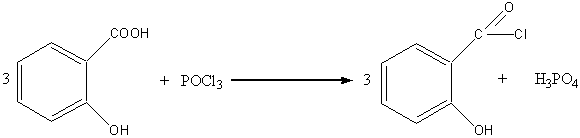
С хлороксидом фосфора салициловая кислота образует хлорангидрид салициловой кислоты:
При взаимодействии этого хлорангидрида с фенолом образуется фениловый эфир салициловой кислоты (фенилсалицилат, tпл.=43оС), который под названием салол используется в медицине как дезинфицирующий препарат при кишечных заболеваниях и примечателен тем, что в кислой среде желудка не гидролизуется, а распадается только в кишечнике:
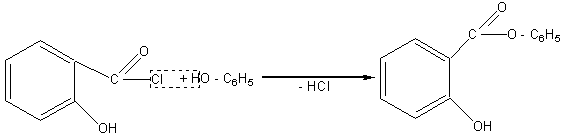
фенилсалицилат (салол)
В промышленности салол получают нагреванием салициловой кислоты и фенола в среде хлороксида фосфора.
Бензольное ядро салициловой кислоты может вступать в реакции электрофильного замещения с галогенами, азотной, серной кислотами и другими электрофильными реагентами. За счет влияния ОН-группы ароматическое ядро салициловой кислоты значительно активнее к этим реакциям, чем бензольное ядро молекулы бензойной кислоты. Так, салициловая кислота легко взаимодействует с бромной водой, тогда как бензойная кислота в этих условиях бромную воду не обесцвечивает:
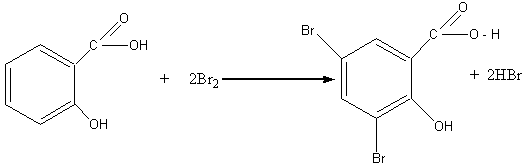
3,5-дибромсалициловая кислота
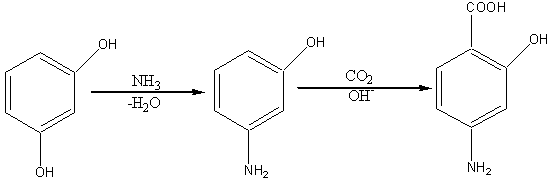
Из других производных салициловой кислоты большое значение имеет n-аминосалициловая кислота (4-амино-2-гидроксибензойная), которая сокращенно называется ПАСК. Исходным веществом для получения этой кислоты служит резорцин, который сначала действием аммиака превращает в мета-аминофенол, и потом уже карбоксилированием последнего по реакции Кольбе-Шмитта – в ПАСК:
|
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.