4) Рассчитать конечное содержание серы (%) в жидкой стали до и после раскисления алюминием, находящейся в равновесии со шлаком заданного состава. Содержанием серы в шлаке пренебречь. Определить степень десульфурации, %. Сделать выводы о влиянии окисленности стали на эффективность десульфурации.
Решение варианта № 0.
Окисленность жидкой стали контролируется элементом, обеспечивающим наименьшую равновесную активность кислорода по соответствующей реакции раскисления. Для того чтобы определить какой из элементов контролирует окисленность металла, необходимо рассчитать активность кислорода, находящегося в равновесии с каждым элементом жидкой стали.
Для варианта № 0 окисленность жидкого металла может контролироваться углеродом или кремнием. Активность кислорода, находящегося в равновесии с углеродом, можно найти по реакции
![]() (4.1)
(4.1)
![]() .
(4.2)
.
(4.2)
В открытом агрегате справедливо РСО ≈ 1 атм. При 1600 °С константа равновесия реакции (4.1) равна КСО = 499 (см. приложение Е). Активность углерода можно найти по заданному составу жидкой стали (для варианта № 0 [C] = 0,30%, [Si] = 0,45%). Коэффициент активности углерода можно найти при помощи массовых параметров взаимодействия. При этом температурную зависимость параметров взаимодействия можно учесть в приближении теории регулярных растворов
![]() или
или ![]() .
(4.3)
.
(4.3)
В случае состава стали варианта № 0 коэффициент активности и активность углерода с учётом параметров из приложения 5 равны
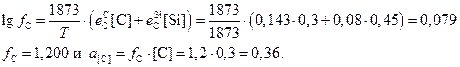
Подставляя а[C] в (4.2)
![]() .
.
Равновесную с кремнием активность кислорода можно найти по реакции
![]() (4.4)
(4.4)
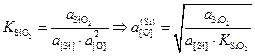 . (4.5)
. (4.5)
Допустим, что при
взаимодействии кремния с кислородом в объеме металла образуется чистое твердое
соединение SiO2
и ![]() . При 1600 °С константа
равновесия реакции (4.4) равна
. При 1600 °С константа
равновесия реакции (4.4) равна ![]() (см.
приложение Е). Коэффициент активности и активность кремния с учётом параметров
из приложения 5 равны
(см.
приложение Е). Коэффициент активности и активность кремния с учётом параметров
из приложения 5 равны
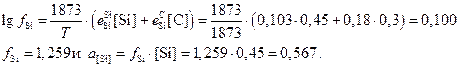
После подстановки значения а[Si] в (4.5) получим
![]() .
.
Так как ![]() , то окисленность жидкой стали
контролируется кремнием.
, то окисленность жидкой стали
контролируется кремнием.
Для того, чтобы
найти содержание кислорода, в равновесии с кремнием, необходимо рассчитать значение
коэффициента активности кислорода. Сделаем это в приближении, что ![]() , так как концентрация
кислорода пока не известна.
, так как концентрация
кислорода пока не известна.
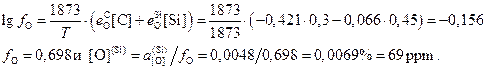
В случае
вакуумирования стали РСО ≈ Рост < 1 атм.
и активность кислорода в равновесии с углеродом будет ниже. При определённом
остаточном давлении в вакуумной камере кремний перестанет контролировать
окисленность жидкой стали, и активность кислорода будет уже определять углерод.
Искомое остаточное давление (давление СО в газовой фазе) можно найти из
равенства ![]() . Тогда
. Тогда
![]() ,
(4.6)
,
(4.6)
Подставив значения
![]() в (4.6), получим
в (4.6), получим
![]()
Таким образом, при остаточном давлении в вакуумной камере ниже 0,862 атм. контролировать окисленность жидкой стали будет углерод. То есть при дальнейшем понижении давления именно углерод, а не кремний будет определять концентрацию кислорода в металле. Более того, углерод при этом будет восстанавливать включения SiO2.
При добавлении в жидкую сталь алюминия, как правило, именно он определяет окисленность, связывает кислород в прочные соединения и, таким образом, раскисляет металл. Равновесное содержание кислорода при раскислении стали алюминием можно найти по реакции
![]() (4.7)
(4.7)
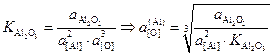 . (4.8)
. (4.8)
При раскислении стали
алюминием (0,01…0,05% Al) образуется
чистое твердое соединение Al2O3
и ![]() . При 1600 °С константа
равновесия реакции (4.7) равна
. При 1600 °С константа
равновесия реакции (4.7) равна ![]() (см.
приложение Е). Коэффициент активности и активность алюминия с учётом параметров
из приложения Д равны
(см.
приложение Е). Коэффициент активности и активность алюминия с учётом параметров
из приложения Д равны
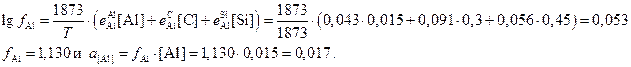
Подставляя значения
![]() в (4.8), получаем
в (4.8), получаем
![]() .
.
Для того, чтобы найти содержание кислорода необходимо рассчитать коэффициент активности кислорода
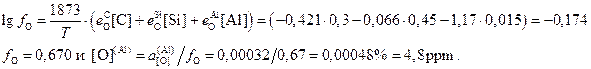
Неметаллические включения, которые образуются при добавлении алюминия, принято называть первичными. Количество первичных включений можно рассчитать по разнице содержаний кислорода до и после добавления алюминия. При этом необходимо учесть, что в одной молекуле включения глинозёма (Al2O3) содержится три атома кислорода
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.